“O senhor escreveu que as pessoas com NF1 toleram menos o calor e depois falou sobre convulsões e febre. Como saber se uma criança com NF1 está com calor ou febre? ” TR, do Rio de Janeiro.
Cara T, obrigado pela sua excelente pergunta, pois ela me permite explicar melhor as diferenças entre os sinais físicos de uma pessoa com calor ou com febre.
Calor
Começo pela pessoa que ficou exposta a um ambiente quente durante certo tempo realizando uma atividade física qualquer, ou um esporte ou um trabalho braçal. À medida que absorvemos o calor do ambiente (por exemplo, dos raios solares), nosso corpo vai aquecendo e sua temperatura aumenta. Quando fazemos atividades físicas, os músculos produzem calor e também aquecem o nosso corpo. Se somarmos as duas fontes de calor, ambiente quente e exercício físico, nosso corpo aumentará ainda mais rapidamente a sua temperatura.
Sabemos que nosso cérebro só funciona bem dentro de uma faixa normal de temperatura. Quem desejar saber mais sobre este assunto pode ver meu livro para crianças chamado “Cabeça fria é que faz gol” (AQUI).
Para manter a temperatura do cérebro dentro da faixa saudável, o corpo distribui uma parte do sangue sob a pele e começa a suar. Por isso a nossa pele fica avermelhada pelo sangue (chamada de rubor) e umedecida pelo suor. Se você colocar um termômetro na axila desta pessoa suando e com a pele quente, especialmente nas extremidades (mãos e pés, que continuam secos), poderá encontrar a temperatura um pouco aumentada, como se fosse febre, mas não é. É aumento da temperatura do corpo por causa do ambiente e/ou do exercício.
Se o suor evaporar, a evaporação retira calor da pele, que resfria o sangue, que então resfria o cérebro. Se o suor não puder evaporar, como nos ambientes úmidos (da floresta amazônica, por exemplo), o calor vai acumulando e aquecendo o cérebro e prejudicando as suas funções a partir de uma certa temperatura, geralmente acima de 40 graus centígrados.
O nível de tolerância de uma pessoa ao aumento da sua temperatura cerebral depende de quanto está acostumada com o ambiente quente e com o exercício (condicionamento) e de seu estado de saúde. Diversas doenças, incluindo a NF1, reduzem a tolerância das pessoas ao aumento do calor corporal.
Febre
No aumento do calor corporal por causa do ambiente e do exercício nosso corpo QUER jogar calor para fora e baixar a temperatura, mas NÃO CONSEGUE. Ao contrário, na febre, o corpo QUER conservar calor para aumentar a temperatura e assim combater a infecção que o está atingindo, possivelmente atrapalhando o crescimento de algumas bactérias.
Então, na febre, o organismo vai fazer ao contrário do que no ambiente quente: vai retirar o sangue da pele, para evitar a perda de calor para o ambiente, e por isso ficamos pálidos. Além disso, enquanto a febre estiver subindo, o corpo não vai suar. Se estas duas tentativas não forem suficientes para aumentar a temperatura em 1 ou 2 graus, o indivíduo começa a tremer para produzir calor por meio de contrações musculares involuntárias.
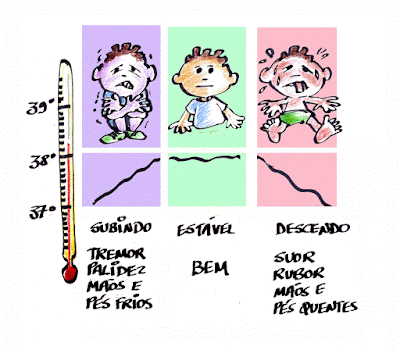
Esta é a primeira fase, na qual a febre está subindo (ver figura acima). Nesta fase as pessoas sentem frio, calafrios e outras manifestações de desconforto, fadiga e desânimo. Esta fase pode durar alguns minutos ou mesmo horas, dependendo da doença que está causando a febre.
Assim que o acúmulo de calor atinge a temperatura corporal que a evolução selecionou como sendo a mais adequada para aquela infecção, a palidez melhora, o tremor desaparece e a pessoa se sente mais confortável, apesar de estar com a temperatura interna acima de 38 graus centígrados. Esta é a fase estável de febre (ver figura acima), e pode durar várias horas.
No momento em que o organismo entende que a causa da febre diminuiu (a produção de certas proteínas pelas bactérias ou pelas células que combatem a infecção), começa então a última fase da febre, na qual o corpo tenta eliminar o excesso de calor que acumulou nas fases anteriores. Neste momento começa a vermelhidão da pele, a produção de suor e a sensação de calor que faz com que as pessoas retirem as cobertas e as roupas quentes (ver figura acima).
Tratamentos?
Dependendo do aumento da temperatura corporal causado por ambiente quente e exercício, ele precisa ser combatido com medidas urgentes como interromper a atividade física e retirar a pessoa do calor, dar banhos de água fria e acomodá-la em ambiente com ar condicionado. Algumas vezes estas medidas podem ser de emergência, pois a insolação (ou hipertermia) pode ser fatal ou deixar graves sequelas.
Outras formas raras de aumento da temperatura corporal, chamadas hipertermias malignas, que ocorrem por sensibilidade a determinados medicamentos, especialmente anestésicos, devem ser tratadas intensivamente pois podem ser fatais.
Por outro lado, estou convencido cientificamente de que não há necessidade de tratarmos a febre comum, causada por infecções bacterianas e virais, porque ela segue seu curso natural das três fases descritas acima, mesmo nas crianças que apresentaram algum episódio de convulsão febril (ver aqui). A febre em si não causa qualquer dano, pois ela geralmente é autolimitada a menos de 40 graus, ou seja, abaixo dos limites para causar problema cerebral.
Uma exceção que justifica o tratamento da febre alta seria para aquelas pessoas com insuficiência cardíaca grave, pois o aumento do metabolismo causado pelos tremores musculares poderia ser o bastante para descompensar a função cardíaca que já está muito limitada.
Além disso, a primeira fase da febre costuma durar menos tempo do que o tempo necessário para um antitérmico por via oral fazer seu efeito (a não ser os injetáveis). Também não faz sentido tratar a febre na sua fase dois, em que ela está estável, já atingiu seu limite natural e a pessoa já está mais confortável. Menos necessário ainda seria o tratamento na terceira fase da febre, na qual ela está espontaneamente desaparecendo.
Parece-me que muitas vezes damos os medicamentos antitérmicos apenas para aliviar os sintomas de desconforto e fadiga causados pela febre. No entanto, estes sintomas são restritos apenas à fase inicial da febre e fazem parte das defesas do organismo para ficarmos mais quietos e protegidos num momento em que nosso corpo está empenhado no combate à infecção.