“Meu filho foi diagnosticado com autismo e depois descobrimos que ele tem Neurofibromatose do tipo 1. É possível ter as duas doenças ou o autismo é uma complicação da NF1? ” AGR, de Florianópolis, SC.
Cara A, obrigado pela sua pergunta, pois ela pode ser útil a muitas famílias com pessoas com Neurofibromatose do tipo 1.
O que é o autismo?
O autismo é uma doença que afeta o desenvolvimento global neurológico e se caracteriza por dificuldades na comunicação social e na interação com outras pessoas e por padrões de comportamento repetitivos e restrição dos interesses.
Assim como na NF1, há grande variação nas manifestações clínicas do autismo, por isso hoje adotamos o nome mais abrangente de Transtorno no Espectro do Autismo.
O diagnóstico do autismo vem aumentando: em 2004, a cada 160 crianças que nasciam uma delas era diagnosticada com autismo, mas atualmente para cada 60 crianças nascidas uma delas apresentará o diagnóstico de autismo. Portanto, o autismo é muito mais comum do que a NF1, pois a cada três mil crianças que nascem apenas uma delas apresentará a NF1.
É preciso uma avaliação cuidadosa para termos certeza de que uma criança apresenta mesmo o autismo. Quando se usam questionários respondidos pelos pais, o diagnóstico de autismo é mais frequente do que quando as crianças são avaliadas diretamente por especialistas (psicólogos e psiquiatras).
Com este cuidado em mente, há estudos científicos mostrando que entre 11 e 29% das crianças com NF1 apresentam comportamentos que são parecidos com os comportamentos das pessoas com autismo. É comum na NF1 encontrarmos atrasos na fala, desatenção, impulsividade e dificuldades de comunicação social.
Diagnóstico do autismo
Deve ser feito por psicólogos, psiquiatras e pediatras especializados, que usam testes sobre o funcionamento cognitivo, informações dos pais e cuidadores e observação direta das crianças.
O diagnóstico de autismo na presença de NF1 (e de outras doenças genéticas) pode ser mais difícil porque algumas crianças com NF1 apresentam sinais e sintomas que são muito parecidos com aqueles encontrados nas pessoas com autismo.
Em alguns casos mais raros (cerca de 1 em cada 300 mil pessoas) a criança pode realmente apresentar as duas doenças ao mesmo tempo.
Antes de seguir adiante com a busca por um especialista, podemos lembrar alguns comportamentos que são característicos das crianças com autismo:
- Dificuldade em manter o contato visual
- Atraso importante na fala
- Pouco uso de gestos (não costumam apontar coisas, mostrar objetos, aplaudir ou acenar)
- Não respondem quando chamadas pelo nome
- Não chamam a atenção de outras pessoas para objetos
- Apresentam forte interesse por determinados objetos ou brincam de forma repetitiva com objetos
- Grande sensibilidade a estímulos (sonoros e outros)
Se você acha que sua criança apresenta vários destes sintomas, você deve procurar um especialista para confirmar ou não o diagnóstico de autismo.
Diferenças entre autismo e NF1
Há poucos estudos científicos sobre autismo e NF1 com crianças muito pequenas, por isso nosso conhecimento ainda é um pouco limitado para os primeiros anos de vida (ver ao final deste texto um estudo realizado na Inglaterra).
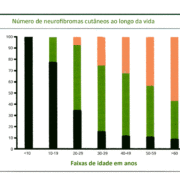
As dificuldades sociais das pessoas com autismo estão presentes desde o começo da infância, enquanto as dificuldades sociais das pessoas com NF1 parecem aumentar ao longo da vida, especialmente na adolescência.
Minha impressão pessoal é de que a principal diferença clínica entre NF1 e autismo seria as crianças com NF1 apresentarem maior ligação afetiva com pais e outras pessoas do que as crianças com autismo.
Um estudo recente (2021) investigou as respostas do sistema nervoso de crianças com NF1 (processamento auditivo) e comparou estes resultados com o padrão encontrado em crianças com autismo. Ver aqui estudo completo em inglês: CLIQUE AQUI
Tratamentos
Mesmo que sua criança com NF1 tenha apenas alguns comportamentos parecidos com autismo, ela poderá se beneficiar de alguns tratamentos que são ofertados às crianças com autismo, que buscam melhorar as habilidades cognitivas e sociais.
Mais informações sobre o autismo
Veja a belíssima cartilha feita pelo ZIRALDO sobre o autismo aqui: http://www.mpsp.mp.br/portal/page/portal/cao_civel/cartilha-ziraldo-autismo-uma-realidade.pdf
Você pode encontrar mais informações sobre o autismo na Associação Brasileira de Autismo: http://www.autismo.org.br/site/#
Um estudo importante
Em 2013 foram publicados os resultados de um estudo científico realizado na Inglaterra sob a coordenação da Dra. Susan Huson, intitulado “Neurofibromatose do tipo 1 e desordem no espectro do autismo” (Garg S, Green J, Leadbitter K, Emsley R, Lehtonen A, Evans DG, Huson SM. Neurofibromatosis type 1 and autism spectrum disorder. Pediatrics. 2013;132(6):e1642-8. doi:10.1542/peds.2013-1868).
O estudo procurou determinar a prevalência, ou seja, o número de pessoas afetadas por comportamentos no espectro do autismo (ASD) entre as pessoas com NF1.
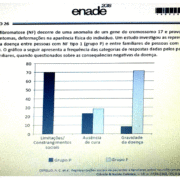
Os autores utilizaram todos os casos de NF1 registrados numa área da Inglaterra habitada por uma população de 4,1 milhões de ingleses. De um total de 109 (52,7%) pessoas que responderam ao questionário SRS (Social Responsiveness Scale), elas foram agrupadas como: ASD significativo: 32 pessoas, ASD moderado: 29 pessoas, sem ASD: 48 pessoas.
Uma amostra de cada um destes grupos formados pelo questionário foi examinada pessoalmente para confirmação ou não do ASD por meio de testes e exames realizados por especialistas.
Os resultados finais mostraram que das 47 pessoas que foram submetidas aos testes e especialistas, 29,5% apresentava ASD confirmado, 27,7% apresentava ASD no limite, e 42,5% não apresentava comportamentos no espectro do autismo.
O grupo com ASD confirmado possuía mais meninos do que meninas, mas não apresentava outras diferenças com os demais grupos (inteligência, nível social, padrão de herança da NF1, gravidade da doença, nível educacional).
Em conclusão, os cientistas encontraram uma prevalência na população de cerca de 45% de pessoas com NF1 apresentando algum grau de comportamento no espectro do autismo.
O estudo recomendou novas pesquisas em busca de tratamentos clínicos para estes comportamentos no espectro do autismo para as pessoas com neurofibromatose do tipo 1.