A equipe médica do Centro de Referência em Neurofibromatoses do HC-UFMG está preparando uma opinião bem estruturada sobre o medicamento selumetinibe. Enquanto isso, as informações abaixo são importantes para compreendermos melhor a questão do tratamento dos neurofibromas plexiformes.
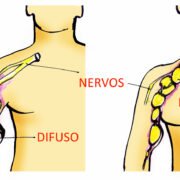
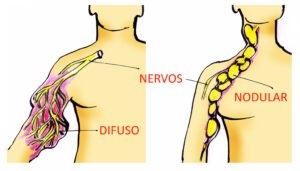
Para começar, precisamos lembrar a definição de neurofibromas plexiformes: são tumores benignos, geralmente congênitos (já estão presentes na criança dentro do útero), formados em vários feixes de nervos e que às vezes se estendem a outros órgãos ou tecidos ao redor.
Geralmente, os neurofibromas plexiformes apresentam mais de 3 cm de diâmetro, enquanto os neurofibromas cutâneos raramente atingem 3 cm de tamanho.
Eles podem surgir e se tornarem visíveis na cabeça, pescoço, tronco ou extremidades (braços e pernas), ou ainda se formarem profundamente nessas mesmas regiões sem serem visíveis.
Em 100 pessoas com NF1, cerca de 50 delas apresentam neurofibromas plexiformes, sendo metade (25) do tipo difuso (que são macios, pouco definidos e de formas irregulares) e metade (25) do tipo nodular (firmes, bem definidos e de forma ovalada) (ver figura acima).
Uma mesma pessoa pode apresentar ambos os tipos de neurofibromas.
Para dizer se um medicamento é eficiente ou não para tratar os neurofibromas, temos que saber como os neurofibromas se comportam sem qualquer tratamento.
Isto se chama história natural dos neurofibromas: como aparecem, como crescem, quais os sintomas e problemas que produzem.
Hoje vamos procurar entender algumas perguntas sobre a história natural do tamanho dos neurofibromas plexiformes (não discutiremos hoje os sintomas e complicações).
Consideramos que um neurofibroma está em crescimento quando ele aumenta em volume mais do que a taxa normal de crescimento corporal da criança.
Então, nossas perguntas são:
- Quando aparecem os neurofibromas plexiformes?
- Os plexiformes sempre aumentam de tamanho? Ou podem permanecer estáveis? Ou podem diminuir com o passar do tempo?
- Qual é a taxa de crescimento anual dos neurofibromas?
- Neurofibromas plexiformes difusos se comportam da mesma forma que neurofibromas nodulares?
- A idade, sexo e/ou raça da pessoa com NF1 influencia o crescimento dos neurofibromas plexiformes?
Um estudo muito interessante sobre algumas destas questões foi publicado em março de 2020 pela Dra. Srivandana Akshintala em colaboração com o grupo da pesquisadora norte-americana Brigitte Widemann (o mesmo grupo que testou o selumetinibe e cujos resultados serviram de base para a aprovação do medicamento pela FDA nos Estados Unidos).
Uma tradução adaptada do título deste estudo pode ser: “Avaliação do crescimento dos neurofibromas plexiformes nodulares e difusos ao longo dos anos, em crianças e adultos jovens com NF1.” (trabalho completo em inglês VER AQUI )
As ideias para este estudo surgiram há cerca de 15 anos e, entre 2008 e 2015, 138 pessoas com NF1 e neurofibromas plexiformes inscreveram-se como voluntárias e foram acompanhadas por cerca de 6 anos, com avaliações clínicas periódicas e medidas do volume dos tumores por ressonância magnética. Ao final, os dados de 122 pessoas puderam ser analisados.
Os resultados do estudo da Dra. Akshintala permitiram responder a algumas das perguntas que mencionamos acima.
No entanto, precisamos lembrar que estes casos podem não representar a população com NF1 como um todo, pois podem ter sido selecionados os casos mais graves.
- Quando aparecem?
Os neurofibromas plexiformes difusos são diagnosticados precocemente na infância (primeira ressonância em geral é realizada em torno dos 8 anos) e os neurofibromas plexiformes nodulares são diagnosticados geralmente mais tarde (primeira ressonância em torno dos 15 anos).
- Como se comportam?
Nossa compreensão atual é de que há grande variabilidade no comportamento dos neurofibromas plexiformes.
Há neurofibromas plexiformes que apresentam fases de crescimento e fases de estabilidade e alguns podem regredir em tamanho sem qualquer tratamento.
Neste estudo da Dra. Akshintala e colaboradores, a maioria dos tumores cresceu em algum momento (ou seja, aumentaram de volume mais do que a taxa normal de crescimento corporal da criança) durante o período de observação.
Em 85 de cada 100 plexiformes difusos houve crescimento ou fases de crescimento e em 76 em cada 100 plexiformes nodulares também houve fases de crescimento durante o estudo.
Ou seja, a maioria dos neurofibromas plexiformes em crianças e adolescentes apresenta fases de crescimento.
Interessante foi saber que em 47 dos 113 neurofibromas plexiformes difusos, o volume final foi menor do que o volume máximo durante o estudo. Ou seja, cerca de 40 em cada 100 tumores ou não cresceram ou até reduziram seu volume, sem tratamento.
Em 10 destes 47 plexiformes difusos (ou seja 1 em cada 4) que não cresceram ou reduziram, houve redução espontânea confirmada, ou seja, o volume final foi menor do que o inicial.
Entre os plexiformes nodulares, a redução espontânea também ocorreu.
Em 12 de 81 plexiformes nodulares, o volume final foi menor do que o volume máximo durante o estudo. Ou seja, cerca de 15 em cada 100 tumores cresceram e depois reduziram seu volume sem tratamento.
Em 7 destes 12 plexiformes nodulares (ou seja 1 em cada 2), houve redução espontânea confirmada, ou seja, o volume final foi menor do que o inicial.
Assim, cerca de 1 em cada 10 neurofibromas plexiformes apresentaram alguma redução espontânea e outros 3 em cada 10 não apresentaram crescimento importante ao final do estudo.
Em conclusão, diante de uma criança ou adolescente com neurofibromas plexiformes, podemos suspeitar que haverá fases de crescimento do tumor, mas não podemos afirmar com certeza o que irá acontecer nos próximos 3 anos.
- Qual a taxa de crescimento?
A taxa de crescimento varia muito entre duas pessoas com NF1 e entre dois plexiformes na mesma pessoa, mas cada tumor apresenta uma certa constância de crescimento na mesma pessoa.
Além disso, a taxa média de crescimento foi muito diferente entre nodulares e difusos: os plexiformes difusos cresceram 19% ao ano e os plexiformes nodulares cresceram 44% ao ano.
- Idade, o sexo e a raça afetam os plexiformes?
A idade, sim, pois as maiores taxas de crescimento dos plexiformes difusos ocorrem na infância, antes dos 5 anos de idade.
Já os neurofibromas nodulares não dependem muito da idade, mas parecem crescer mais a partir da adolescência.
Não foram percebidos efeitos importantes do sexo nem houve diferença entre brancos e não-brancos na taxa de crescimento dos plexiformes.
Conclusão
Este estudo trouxe algumas informações sobre a evolução dos neurofibromas plexiformes:
- Neurofibromas plexiformes difusos parecem ter uma biologia diferente dos plexiformes nodulares.
- A maioria dos difusos cresce na infância e os nodulares crescem mais tarde.
- Cerca de um em cada dez neurofibromas plexiformes pode regredir espontaneamente sem tratamento.
Estas informações são muito importantes na avaliação do impacto do selumetinibe sobre estes tumores. Em breve, divulgaremos mais sobre esta questão.
Observação: o Dr. Vincent Riccardi tem proposto há muitos anos uma distinção entre os neurofibromas difusos (chamados de epineurais) e os neurofibromas nodulares (chamados de perineurais), os quais possuem origens embriológicas distintas, diferentes momentos de crescimento, diferentes padrões vasculares e possíveis diferenças nas barreiras teciduais à perfusão de medicamentos ( VER AQUI ).