Dra. Vanessa Waisberg recebendo o Prêmio Varilux pelo seu trabalho científico.
A médica e oftalmologista Vanessa Waisberg apresentou sua tese de doutorado, e foi aprovada por unanimidade, no dia 1 de fevereiro de 2019, no Programa de Pós-Graduação em Medicina Molecular da Faculdade de Medicina da Universidade Federal de Minas Gerais.
O título de seu estudo foi: “Alterações genéticas e oftalmológicas na neurofibromatose do tipo 2” e a banca examinadora foi formada por seis professores com doutorado em oftalmologia, genética, clínica médica e medicina molecular. Foram eles, a orientadora Débora Marques de Miranda (orientadora), Luiz Oswaldo Carneiro Rodrigues (co-orientador), Márcio Bittar Nehemy (co-orientador), Daniel Vitor de Vasconcelos Santos, Galton Carvalho Vasconcelos, Juliana Garcia Carneiro, Antônio Marcos Alvim Soares Junior e teve como suplente Marco Aurélio Romano.
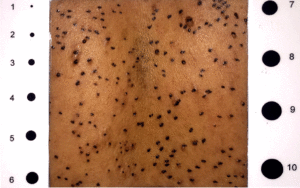
A Dra. Vanessa Waisberg mostrou que o exame oftalmológico especializado utilizando a tomografia de coerência óptica permitiu a identificação de sinais específicos nos olhos das pessoas com NF2. Estes sinais foram correlacionados com as alterações genéticas encontradas no exame do DNA e esta associação permitiu uma melhor definição do diagnóstico e orientação do prognóstico da doença em cada pessoa examinada. Além disso, o estudo apresentou três novas mutações patológicas do gene NF2 que ainda não haviam sido descritas.
Parte dos resultados já foram comentados neste site da AMANF (VER AQUI) e publicados numa das melhores revistas mundiais de Oftalmologia (artigo em inglês VER AQUI ). Além disso, foram apresentados e citados no Congresso Mundial sobre Neurofibromatoses realizado em Paris em novembro de 2018 e receberam o principal prêmio para trabalhos científicos em Oftalmologia, o Prêmio Varilux (reportagem do Jornal Brasileiro de Oftalmologia: VER AQUI). O restante dos resultados deve ser publicado em breve.
Durante a defesa da sua pesquisa, os resultados da Dra. Vanessa Waisberg foram comentados por todos os membros da banca, que elogiaram o seu trabalho e fizeram sugestões e críticas importantes que serão incorporadas ao texto final a ser impresso para o banco de teses de doutorado da UFMG.
É importante lembrar que a Dra. Vanessa realizou a defesa de sua tese com clareza, boa disposição e bom humor, considerando que ela está esperando seu segundo filho para os próximos dias. Desejamos toda a felicidade para ela e sua família e estamos esperando seu retorno ao trabalho após a merecida licença maternidade.
Para finalizar, durante a banca, li a carta abaixo.
Empatia, Ética e Emoção
Sinto-me honrado por participar deste grupo de cientistas que avaliam o estudo da Dra. Vanessa Waisberg sobre alterações oculares e genéticas em pessoas com Neurofibromatose do tipo 2 (NF2).
Enquanto ela desenvolvia sua pesquisa nestes últimos anos, como co-orientador do seu doutorado, pude observar sua grande capacidade profissional como médica e oftalmologista e suas exemplares qualidades pessoais.
Uma banca de doutorado tem por meta avaliar diversas habilidades da doutoranda, muito além das virtudes científicas da pesquisa realizada. A originalidade, a adequação dos métodos, a confiabilidade dos resultados, a pertinência da discussão e o impacto do conhecimento gerado devem ser objeto de apreciação da banca. No entanto, este papel da análise do estudo realizado durante o doutorado muitas vezes vem sendo realizado pelas revistas científicas, permitindo que a banca possa se dedicar à avaliação das outras qualidades da doutoranda.
Devo, então, examinar alguns critérios que indicam a plena capacidade da Dra. Vanessa Waisberg para receber o título de Doutora, o qual significa que ela estará habilitada para realizar pesquisas científicas de forma autônoma assim como ensinar ciência. É esta capacitação da Dra. Vanessa Waisberg que desejo comentar.
Observei o compromisso da Dra. Vanessa Waisberg com a busca pela verdade científica enquanto reuníamos pessoas voluntárias acometidas pela NF2, as quais foram submetidas a avaliações clínicas, oftalmológicas e genéticas que resultaram em novas informações relevantes e inéditas para o cuidado médico com portadores de NF2 e suas famílias.
Informações cientificamente obtidas são fundamentais numa época em vivemos, na qual a verdade vem sendo relativizada, numa onda anti-civilizatória patrocinada por líderes populistas em várias partes do mundo. Enfrentamos hoje uma cultura demagógica na qual as versões pessoais e subjetivas, construídas pelas paixões políticas, alcançam o mesmo valor que a opinião construída por especialistas a partir de fatos e pesquisas.
Informações científicas verdadeiras deveriam constituir a maior riqueza contemporânea, pois são a única alternativa para que a humanidade resolver suas questões de sobrevivência num planeta ameaçado pelo aquecimento global e pela desigualdade econômica.
Foi em busca de informação científica que a Dra. Vanessa Waisberg utilizou tecnologia de ponta na oftalmologia e na genética para estudar as pessoas com NF2. Sua contribuição passa a integrar a enorme quantidade de dados científicos que são disponibilizados mundialmente a cada dia.
Informações em grande escala, os chamados big data, permitem a construção de sistemas de inteligência artificial, um recurso tecnológico em expansão, que pode ajudar a medicina a enfrentar as doenças, em especial aquelas mais de cinco mil doenças raras, entre elas a NF2.
A inteligência artificial já permite à medicina aumentar sua precisão nos diagnósticos e a descoberta de novos tratamentos. Alguns sistemas de inteligência artificial já superam seres humanos no diagnóstico e algoritmos para tratamento de muitas doenças.
No entanto, apesar do enorme potencial da inteligência artificial, como aprendi com o cientista da computação Juliano Viana, ela não pode, pelo menos por enquanto, superar o ser humano em três campos: da empatia, da ética e da emoção. São justamente estes três aspectos que desejo relembrar do convívio no trabalho com a da Dra. Vanessa Waisberg.
Primeiro, mesmo sabendo que a NF2 é uma doença rara, Dra. Vanessa Waisberg demonstrou empatia para com a questão científica de grande importância para as pessoas e suas famílias com a doença, que é saber se podemos melhorar nossa capacidade diagnóstica e prognóstica da NF2. Ela abraçou a pergunta com entusiasmo e se dedicou a inúmeras horas de estudo numa revisão extensa da literatura. Seu esforço resultou num método de pesquisa que respondeu afirmativamente, sim, podemos aumentar a segurança do diagnóstico e orientar melhor o tratamento e o prognóstico.
Na condução de sua pesquisa, a Dra. Vanessa Waisberg se pautou pela ética, refletindo cuidadosamente a cada passo sobre as consequências de seus atos como médica e cientista. Se estamos diante do resultado de um exame genético de uma pessoa, quantos desdobramentos de nossa informação sobre sua vida podemos prever? Posso testemunhar que a Dra. Vanessa agiu com todo o cuidado necessário numa pesquisa envolvendo informações genéticas.
Finalmente, acompanhei a emoção da Dra. Vanessa Waisberg diante das pessoas com NF2, tanto na coleta dos dados quanto na entrega dos resultados, quando irradiava discretamente sua felicidade com os resultados com melhor prognóstico e visivelmente se comovia solidária com os casos mais graves. Sua solidariedade traduziu-se também no compromisso ético de dar continuidade ao pronto acompanhamento oftalmológico gratuito para as pessoas com NF2 que se voluntariaram para a sua pesquisa.
Portanto, em conclusão, é com enorme alegria que reconheço na Dra. Vanessa Waisberg todas as qualidades necessárias, acadêmicas, científicas, éticas e humanitárias, para seu título de Doutora.
Parabéns e longa vida dedicada à construção da Ciência.
LOR
Fevereiro de 2019