Algumas pessoas têm perguntado se a equipe médica do Centro de Referência em Neurofibromatoses do Hospital das Clínicas da Universidade Federal de Minas Gerais (CRNF) tem “conhecimento e expertise” sobre o medicamento selumetinibe (nome comercial Koselugo).
Sim, temos conhecimento sobre os estudos realizados e temos indicado o seu uso em determinadas condições de acordo com os critérios abaixo:
QUANDO USAR O SELUMETINIBE?
Devo usar o novo medicamento? Como faço para conseguir o novo medicamento para neurofibromatose? Como devo usar? Quanto custa?
Estas são as perguntas mais frequentes que temos recebido nos últimos meses, desde que o selumetinibe foi aprovado nos Estados Unidos para o tratamento de determinados casos de neurofibromas plexiformes sintomáticos e inoperáveis.
Primeiro, você sabe o que é o selumetinibe?
É um medicamento do tipo antineoplásico, que é como um tipo de quimioterapia, da classe dos inibidores de MEK, estudados e usados geralmente para tratar alguns tipos de câncer.
O selumetinibe é um medicamento de uso por via oral, feito para ser tomado diariamente, que já tem registro no Brasil e bula registrada na Anvisa desde agosto de 2023.
Nós sabemos quanto sofrimento os neurofibromas plexiformes trazem para as pessoas com NF1 e suas famílias.
Por isso, há vários anos, nossa equipe do Centro de Referência em Neurofibromatoses do Hospital das Clínicas da Universidade Federal de Minas Gerais tem estudado profundamente todos os trabalhos científicos que estão sendo publicados sobre o uso do selumetinibe na neurofibromatose tipo 1.
Temos discutido entre nós os resultados encontrados nestes estudos e também com o Dr. Carlos Magno Leprevost, da equipe médica do laboratório fabricante do remédio (AstraZeneca) e com um dos médicos autores da pesquisa que justificou a liberação do medicamento nos Estados Unidos, o Dr. Michael Fisher.
Além disso, participamos do último Congresso Europeu sobre neurofibromatoses agora em dezembro (aqui) e levamos as nossas análises sobre o selumetinibe na forma de dois posters com partes das informações que apresentamos abaixo.
RELÓGIO DE CUIDADOS
Nossa resposta para esta importante questão é apresentar publicamente uma série de cuidados que construímos para que cada pessoa (ou sua família) com NF1 possa entender os efeitos esperados do remédio e decidir junto com seu médico ou sua médica e com segurança se deve usar ou não o selumetinibe e durante quanto tempo.
As etapas que cada pessoa ou cada família deve seguir estão explicadas aqui no blog, um passo a cada post (um post por dia), até completarmos os 12 passos.
A partir de amanhã, iremos seguir passo a passo com você para sabermos se você tem tumores semelhantes aos que foram estudados, o que você espera do selumetinibe e o que ele pode oferecer.
Os passos estão resumidos na figura acima, que ilustra o nosso “Relógio de Cuidados“.
Passo 1 – Tenho um neurofibroma plexiforme?
Como você sabe que tem um neurofibroma plexiforme?
Geralmente as médicas e os médicos com experiência em neurofibromatoses são capazes de identificar um neurofibroma plexiforme desde os primeiros anos de vida, porque eles são congênitos, quer dizer, se formam desde a vida dentro do útero.
Você pode encontrar neste link mais informações sobre o que são e como aparecem e crescem os neurofibromas plexiformes: https://amanf.org.br/2020/10/como-crescem-os-neurofibromas-plexiformes/
Somente se você tem um neurofibroma plexiforme você deve dar os passos seguintes, pois o selumetinibe está indicado apenas para este tipo de neurofibroma.
Não está indicado para neurofibromas cutâneos, gliomas ou outras manifestações da NF1.
IMPORTANTE
Além de saber se você tem um plexiforme, precisamos avaliar se ele está crescendo ou não e se está produzindo sintomas, como dor ou perda de função.
Nas últimas semanas, meses ou anos, seus neurofibromas plexiformes podem ter estado estáveis quanto ao tamanho e sintomas.
Mas se eles estiverem crescendo rapidamente, endurecendo ou manifestando dor e outros sintomas, pode ser que esteja ocorrendo a transformação maligna do neurofibroma, e então você precisa esclarecer esta questão rapidamente.
Então, nosso primeiro passo é afastar a possibilidade de seu plexiforme estar sofrendo transformação maligna.
O selumetinibe não está indicado para neurofibromas com transformação maligna.
Ver aqui mais informações sobre a transformação maligna dos plexiformes: https://amanf.org.br/transformacao-maligna/
Além disso, você precisa saber de algumas situações que não permitem você usar selumetinibe, ou seja, se possui algum dos critérios de exclusão abaixo:
- Se estiver grávida ou amamentando.
Se você for uma adolescente ou mulher em idade com possibilidade de ficar grávida (ou seja, depois da primeira menstruação), deverá fazer um teste de gravidez e iniciar um método anticoncepcional seguro e eficiente antes de usar o selumetinibe.
-
- Se possuir alguma outra doença clínica importante,como infecções, disfunção cardíaca, pulmonar, hepática ou renal.
- Se necessitar de provável cirurgia durante o uso do selumetinibe.
- Estiver realizando radioterapia ou quimioterapia.
- Não puder realizarexames de imagem para reavaliar o tumor.
- Incapacidade de engolir cápsulas.
Então, se você tem um neurofibroma plexiforme, sintomático e inoperável, e não está sofrendo transformação maligna e você não possui nenhum destes critérios de exclusão citados, vamos dar amanhã o passo seguinte para o uso ou não do selumetinibe.
Passo 2 – O que está acontecendo com meu neurofibroma plexiforme?
É importante você saber que diante de um adulto ou uma criança ou um adolescente com neurofibroma plexiforme, podemos suspeitar que haverá fases de crescimento do tumor, outras de estabilidade e até mesmo fases de redução do tumor, mas não podemos afirmar com certeza o que irá acontecer nos próximos anos.
Também precisamos saber qual tipo de neurofibroma plexiforme que você possui, porque existem dois tipos, os difusos e os nodulares e eles se comportam de forma diferente de acordo com a idade da pessoa.
Veja aqui mais informações sobre os neurofibromas plexiformes difusos e nodulares: https://amanf.org.br/2020/10/como-crescem-os-neurofibromas-plexiformes/
A maioria dos plexiformes apresenta algum crescimento na infância e adolescência, acima do crescimento natural da pessoa, mas os difusos crescem mais rapidamente antes da adolescência e os nodulares depois da adolescência.
Podemos dizer 3 coisas importantes sobre o crescimento dos neurofibromas plexiformes:
- Os difusos parecem ter uma biologia diferente dos plexiformes nodulares.
- A maioria dos difusos cresce na infância e os nodulares crescem mais tarde.
- Muitos plexiformes difusos podem reduzir seu tamanho na vida adulta.
Então, nos últimos meses, o seu plexiforme está crescendo, está do mesmo tamanho ou está diminuindo?
Assim, a sua idade pode ser um fator importante para saber se deve ou não usar o selumetinibe. O estudo que serviu de base para a aprovação nos Estados Unidos foi feito com crianças e adolescentes.
Outra questão importante é se o seu neurofibroma plexiforme está causando ou não problemas para sua vida. O selumetinibe foi aprovado nos Estados Unidos para neurofibromas que estejam causando problemas como deformidade, dor ou perda de função e que não possam ser corrigidos por meio de cirurgia.
Se o seu plexiforme está causando problemas para você, então veja o nosso post de amanhã.
Passo 3 – Quais os problemas causados pelo meu neurofibroma plexiforme?
Neste passo, vamos ver os principais problemas e sintomas causados pelos plexiformes que foram tratados com selumetinibe no estudo da Dra. Gross nos Estados Unidos.
Queremos ajudar você a saber o que você pode esperar com o tratamento.
Metade dos plexiformes apresenta uma ou mais das seguintes consequências:
- Deformidades físicas
- Dor
- Perda de alguma função
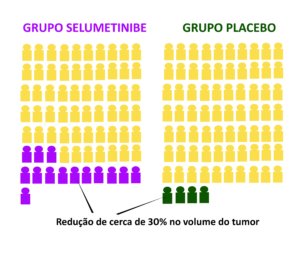
A – Se sua queixa principal sobre o plexiforme for a deformidade física, você precisa saber que no estudo da Dra. Gross e colaboradores (2020) (ver aqui) o selumetinibe reduziu o tamanho do tumor de forma duradoura (mais de um ano de uso constante do medicamento) em 1 em cada 2 crianças (ou adolescentes) que usaram o medicamento.
Nenhuma criança apresentou cura, ou seja, o tumor não desapareceu em nenhuma delas.
Esta redução nestas crianças e adolescentes foi entre 30 e 40% do tamanho inicial, quer dizer, se o plexiforme tinha um volume de um litro, por exemplo, o selumetinibe reduziu cerca de 2 copos aproximadamente.
Você precisa então pensar se esta redução de 30% já seria suficiente para melhorar a deformidade causada pelo plexiforme. Se esta redução faria com que você se sentisse mais confortável porque as outras pessoas estariam percebendo menos o seu plexiforme, por exemplo.
Se você acha que a possível redução de 40% do tumor é suficiente para você enfrentar os riscos e custos do medicamento, vá para o passo seguinte (Passo 4).
B – Se o problema principal causado pelo plexiforme for a dor, que pode ser muito forte em algumas pessoas, você precisa saber que a redução do tamanho do plexiforme observada com o selumetinibe em metade das crianças e adolescentes não foi relacionada com a melhora da dor.
Nós também temos dúvidas se o estudo da Dra. Gross comparou corretamente a dor nas pessoas que usaram o selumetinibe, pois a dor é um sentimento subjetivo e pode ser afetada pelo simples uso de uma cápsula colorida achando que é um remédio, o que chamamos de efeito placebo.
E a Dra. Gross não comparou o selumetinibe com algum comprimido placebo.
Então, se a dor é sua queixa principal, seria interessante você realizar um tratamento rigoroso para a dor, seguindo a escada analgésica (ver aqui) antes de considerar o uso do selumetinibe
Mas se você já tentou esta escada analgésica e não está funcionando, e tem esperança de que o selumetinibe possa reduzir sua dor, vá para o passo seguinte (Passo 4).
C – Por fim, sua queixa principal quanto ao plexiforme pode ser a perda de alguma função. Então vamos ver alguns exemplos das perdas funcionais mais comuns causadas pelos plexiformes.
- Se você apresenta perda do movimento de um braço ou uma perna, por exemplo, você precisa saber que estas perdas são causadas precocemente pelo desenvolvimento do plexiforme desde a vida intrauterina e não há evidência de que elas possam ser modificadas pelo uso do selumetinibe.
Talvez seja melhor você investir em outros cuidados para melhorar sua capacidade funcional.
- Se você apresenta dificuldade para respirar por obstrução das vias aéreaspor causa do plexiforme, o selumetinibe apresentou redução da compressão da traqueia em alguns casos especiais, permitindo a retirada da traqueostomia, e isto pode ser uma indicação para você experimentar o selumetinibe, então vá para o passo seguinte (Passo 4).
- Dificuldade visual por causa de invasão do olho pelo plexiforme, você precisa saber que a presença crônica do plexiforme nas proximidades dos olhos pode realmente obstruir a visão, causar glaucoma (aumento da pressão ocular) ou proptose (deslocamento do globo ocular para fora da órbita). Essas são consequências graves do plexiforme que provavelmente não serão modificadas pelo uso do selumetinibe.
Passo 4 – Uma cirurgia poderia corrigir minha queixa principal quanto ao plexiforme? E o remédio?
Antes de iniciar o tratamento com selumetinibe você precisa consultar uma cirurgiã ou cirurgião para saber se uma cirurgia poderia resolver sua deformidade, sua dor ou sua perda de função causadas pelo neurofibroma plexiforme.
Você deve saber que somente conseguimos remover completamente os neurofibromas pequenos e superficiais, que geralmente não causam grandes problemas. Os maiores e mais profundos, podem envolver estruturas vitais e assim se tornarem impossíveis de remoção completa.
Se o seu neurofibroma plexiforme não puder ser removido cirurgicamente ou a cirurgia não garantir a solução da sua queixa principal, você pode considerar o uso do selumetinibe.
É preciso lembrar que os resultados possíveis do selumetinibe, de acordo com o estudo da Dra. Gross e colaboradores (2020), são:
- Redução do tamanho do tumor, em cerca de 30 a 40%.
- Outros resultados, como redução de dor ou melhora da qualidade de vida, podem ocorrer em uma proporção menor de pessoas,mas não está claro ainda qual o tamanho dessa melhora, quanto tempo ela leva para ocorrer e quanto tempo ela dura.
- A redução no tamanho do tumor não se associou, no estudo, a estes outros resultados. Ou seja, reduzir o tumor não necessariamente leva a bons resultados em outras coisas.
Se você não puder realizar a cirurgia e acha que os efeitos possíveis do selumetinibe podem melhorar sua qualidade de vida, siga para o passo seguinte.
Passo 5 – Minha qualidade de vida vai melhorar?
Qualidade de vida é a soma de diversas coisas: sua capacidade de realizar as tarefas do dia, seu estado psicológico, sua disposição para viver, a ausência de dor ou limitações físicas importantes, a sua autonomia pessoal, além das condições de trabalho, moradia, segurança e perspectiva do futuro.
Ou seja, qualidade de vida envolve diversas avaliações subjetivas sobre nossa vida.
A NF1 e os neurofibromas plexiformes podem afetar nossa qualidade de vida de diversas maneiras, como já comentamos acima nas queixas principais (deformidade, dor e perda de função).
A qualidade de vida das crianças e adolescentes com plexiforme foi estudada pela equipe da Dra. Gross e os resultados mostraram que o uso do selumetinibe por cerca de um ano produziu uma pequena variação positiva na qualidade de vida (especialmente na avaliação dos pais), mas não houve dados suficientes para afirmar que isto tenha acontecido de fato.
Eles observaram que as respostas dos voluntários, aos questionários sobre qualidade de vida, mostraram uma melhora entre 6,7 pontos (crianças) e 13 pontos (seus pais) numa escala de 0 a 100 pontos.
Esta melhora com o selumetinibe é bastante próxima aos limites definidos como mínimos (que são de 4 a 6 pontos) pela comunidade científica internacional (ver aqui mais informações sobre esta questão: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3687260/ e aqui https://pubmed.ncbi.nlm.nih.gov/14616041/
Além da mudança na qualidade de vida com o selumetinibe estar próxima aos limites mínimos de variação, o estudo não envolveu outro grupo de crianças usando um placebo (mesmo problema para a avaliação da dor, já comentado), fazendo com que os dados não sejam suficientes como prova estatística.
Portanto, você deve considerar que o tratamento com selumetinibe provavelmente não terá um GRANDE efeito sobre sua qualidade de vida.
Mas se você deseja saber mais sobre o que esperar do tratamento com selumetinibe, siga para o próximo passo.
Passo 6 – Quais efeitos colaterais posso apresentar com o uso do selumetinibe?
Se você chegou até este passo é porque você provavelmente é uma criança ou adolescente que apresenta um neurofibroma plexiforme, sintomático e inoperável.
Você deve estar sofrendo as complicações do tumor a tal ponto que precisa saber os possíveis efeitos colaterais do selumetinibe, se vale a pena o custo em relação ao benefício.
O trabalho científico da Dra. Gross e colaboradores (NEJM, 2020), que justificou a aprovação do selumetinibe nos Estados Unidos, relatou que 1 em cada 4 crianças teve efeitos colaterais intensos o suficiente para obrigar a redução da dose do medicamento e 1 em cada 10 crianças teve que suspender definitivamente o tratamento por causa de sua toxicidade.
É importante salientar que a redução da dose ou a suspensão do tratamento podem levar à perda da resposta inicial ao remédio e o tumor pode voltar a crescer.
Então, vamos saber o que os inibidores de MEK, como o selumetinibe, podem causar no seu organismo .
Outro trabalho científico (para ver o artigo original em inglês CLIQUE AQUI ) analisou os efeitos colaterais destes medicamentos e a Dra. Laura Klesse e colaboradores (2020) usaram uma graduação da gravidade dos efeitos colaterais, uma tabela usada para avaliar os tratamentos de pessoas que têm tumores malignos (câncer), ou seja, para doenças potencialmente mortais (o que geralmente não é o caso dos neurofibromas plexiformes).
Os resultados mostraram que o uso do selumetinibe causou os seguintes efeitos colaterais mais comuns (graus 1 a 2):
- Disfunção cardíaca em 4 de cada 10 crianças
- Diarreia crônica em 1 em cada 2 crianças
- Fadiga (cansaço) em 1 em cada 2 crianças
- Náusea ou vômitos em 1 em cada 2 crianças
- Infecções nas unhas e pele das mãos e pés em 4 em cada 10 crianças
- Acne (espinhas) em 6 em cada 10 crianças
Assim, se você usar o selumetinibe, terá uma chance grande de apresentar uma ou mais de uma destas complicações.
Sabendo que os efeitos colaterais podem acontecer, é preciso que você tenha um sistema de supervisão e comunicação permanente e direto com a equipe médica, para que ela possa reduzir ou corrigir estas possíveis complicações.
No passo seguinte veremos como deve ser feita a supervisão médica.
Passo 7 – Preciso de supervisão médica para usar o selumetinibe?
Se você chegou até este passo é porque você provavelmente é uma criança ou adolescente (ou os seus familiares) que apresenta um neurofibroma plexiforme, que deve estar sofrendo as complicações do tumor a tal ponto que, depois de informada (o) no post anterior, seria capaz de tolerar os efeitos colaterais do selumetinibe.
Para isso, você precisa ter a garantia de que a equipe médica e alguns exames complementares estarão disponíveis, no tempo necessário, pelo Sistema Único de Saúde (ou autorizados pelo seu convênio durante o seu tratamento), ou você terá recursos financeiros próprios para arcar com estas despesas.
Este sistema de proteção deve funcionar da seguinte forma:
- A equipe médica deve realizar em você exames clínicos periódicos (ver post de amanhã).
- Alguns exames complementares podem ser necessários (por exemplo, ecocardiograma para avaliar a disfunção cardíaca).
- Pode ser preciso utilizar outros medicamentos para tratar as complicações (por exemplo as náuseas, diarreias e vômitos).
- A equipe médica pode precisar ajustar a dose do selumetinibe.
- Você e a equipe médica podem decidir interromper o tratamento por causa dos efeitos tóxicos.
Se você considera que pode contar com a supervisão médica durante o tratamento e poderia suportar estes efeitos colaterais para tentar resolver sua queixa principal em relação ao seu neurofibroma plexiforme, então vá para o passo seguinte.
Passo 8 – Como devem ser as reavaliações periódicas?
Se você chegou até aqui e continua achando que vale a pena usar o selumetinibe, precisa planejar algumas medidas que devem ser tomadas a partir do início do tratamento, para saber se está funcionando ou não para atender os objetivos que você definiu como importantes.
Novamente, vamos recorrer ao estudo da Dra. Gross, que mostrou que a redução do volume do tumor aconteceu a partir de cerca de 8 meses de tratamento e o melhor resultado foi obtido em até 16 meses.
Portanto, além das avaliações médicas necessárias caso ocorra algum efeito adverso, é preciso agendar reavaliações periódicas com a equipe médica para saber como está a evolução dos principais sintomas que motivaram o uso do selumetinibe.
Baseados no estudo da pesquisa da Dra. Gross (página 112 do Protocolo de Pesquisa), seriam necessárias reavaliações antes e durante o tratamento da seguinte forma:
- Exame médico completo(incluindo dados de peso, estatura, etc.)
Antes de iniciar o tratamento
A seguir semanal, nos dois primeiros meses
Depois a cada dois meses até 19 meses
Depois a cada seis meses
-
- Exame de sangue(repetir a cada mês no primeiro ano e depois a cada seis meses)
- Hemograma completo (repetir a cada mês)
- Eletrólitos (sódio, potássio, cloreto), CO2, cálcio, fósforo, magnésio, creatinina, uréia, glicemia, ALT, bilirrubina, proteínas totais e fracionadas, CPK)
- Exame de urina, incluindo o teste de gravidez (72 horas antes do início do selumetinibe) (repetir a cada mês no primeiro ano e depois a cada seis meses)
- Eletrocardiograma e Ecocardiograma
Antes de iniciar o tratamento
Com 3, 6 e 11 meses
Depois, a cada seis meses
- Ressonância magnética tridimensional (a Dra. Gross e equipe informam que apenas a é capaz de perceber as diferenças no tamanho do tumor com a medicação)
Antes de iniciar o tratamento
Com 8 meses e 16 meses
Depois a cada seis meses
Antes de iniciar o tratamento
Com 8 meses e 16 meses
Depois a cada seis meses
É preciso lembrar que infelizmente ainda temos muita dificuldade para fazer estes exames pelo Sistema Único de Saúde (SUS).
Além disso, precisamos considerar a necessidade de sedação e seus riscos em crianças para a realização de alguns destes exames.
Se você dispõe dos recursos (técnicos, financeiros e institucionais) para realizar estas reavaliações periódicas, vamos em frente.
Passo 9 – Critérios para interrupção do selumetinibe.
Se você já considerou todas as questões nos passos anteriores e acha que deve usar o selumetinibe, vamos dar o passo seguinte, que é saber quais são os critérios para interrupção do tratamento, baseados naqueles utilizados no estudo da Dra. Gross e colaboradores (2020).
O tratamento com o selumetinibe deverá ser interrompido por três grupos de motivos:
- A) Antes do início do tratamentocom selumetinibe era um neurofibroma plexiforme que estava crescendo (mais de 20% nos últimos 15 meses) e continuou a crescer durante o tratamento.
O estudo da Dra. Gross e colaboradores mostrou que a suspensão completa do tratamento estava indicada se houvesse progressão (ou seja, aumento do tumor) nos ciclos 5, 9, 13, 17, 21, 25 e depois a cada 6 meses (cada ciclo de tratamento dura cerca de um mês).
- B) Era um neurofibroma plexiforme que não estava crescendo antes de iniciar o selumetinibe, mas não apresentou redução até dois anos de tratamento.
- C) Outros critérios para descontinuidade do tratamentopara pacientes com e sem progressão:
- Administrativos(recusa do paciente, no interesse do paciente segundo seu médico, violação do protocolo, não adesão às normas)
- Toxicidade(que não seja resolvida por redução da dose em 21 dias, ou apareça após suspensão da droga e nova tentativa)
- Evidência de progressãodos três neurofibromas plexiformes mais importantes, seja por indicadores clínicos ou pela ressonância magnética em 3D (nos ciclos 6,11 e a cada 6 ciclos).
- Até duas reduções de dose podem ser consideradasse houver efeitos adversos grau 3 ou mais segundo o NCI Common Terminology Criteria for Adverse Effects abaixo apresentados:
- Elevação de certas enzimas no plasma (transaminases)
- Baixa de alguns minerais e eletrólitos no sangue (hipofosfatemia, hipokalemia, hipocalcemia ou hipomagnesemia corrigidas com suplementação)
- Manchas vermelhas com coceira no corpo (rash cutâneo) controlável com terapia adequada.
- Elevação de uma enzima chamada creatinofosfoquinase (CPK), mesmo que seja assintomática
- Toxicidade gastrintestinal (diarreia, náusea, vômitos) controlável
- Catarata (opacidade do cristalino)
- Ganho de peso maior 20% avaliado caso a caso, considerando a possibilidade de estar ocorrendo retenção de líquidos (edema).
- Toxicidade cardíaca (redução da função ventricular)
- Obstrução urinária
- Descolamento da retina ou trombose venosa da retina
- Pneumonite
Se você se sente devidamente informada (o) sobre quando deve parar o tratamento com o selumetinibe, siga adiante no próximo passo.
Passo 10 – Definição da duração do tratamento
Este é um passo importante, pois você deve estar se perguntando por quanto tempo deve usar o medicamento selumetinibe, caso ele produza uma redução de 30 a 40% do volume do seu neurofibroma plexiforme ou melhore sua dor ou sua disfunção.
Infelizmente, não sabemos ainda esta resposta, pois no estudo da Dra. Gross e colaboradores (2020) as pessoas com plexiformes que responderam ao selumetinbe continuaram em uso por tempo indeterminado.
Algumas pessoas que estavam observando redução do plexiforme e tiveram que suspender a medicação por algum motivo, apresentaram volta do crescimento do tumor. Assim parece que o medicamento teria que ser usado continuamente para sustentar os efeitos positivos observados.
Por outro lado, ainda não sabemos os efeitos do uso prolongado do selumetinibe sobre alguns aspectos importantes da vida das pessoas:
- Qual o impacto do selumetinibe noaprendizado, na função cognitiva, na inteligência?
- Qual a chance do selumetinibe produzir alterações no crescimento, no desenvolvimento sexual e na fertilidade?
- Qual a chance do selumetinibe propiciar o aparecimento de doenças malignas?
Em conclusão, aguardamos novos estudos científicos para podermos responder estas questões com segurança.
Passo 11 – Quanto custa o tratamento com selumetinibe?
Se você chegou até aqui é porque está considerando seriamente o uso do selumetinibe para tratar seu neurofibroma plexiforme sintomático e inoperável, apesar das incertezas e riscos que foram apresentados nos passos anteriores.
Então você deseja saber o preço, ou seja, o custo financeiro do medicamento.
O preço pela CMED, R$ 92.761,64 para 25mg com 60 comprimidos = 61,84 reais por mg de selumetinibe.
Como definimos anteriormente, a duração do tratamento não seria inferior a 12 meses, a não ser que houvesse algum efeito colateral que obrigasse a suspensão da droga, ou o plexiforme voltasse a crescer mesmo com a medicação, o que aconteceu com cerca de metade daqueles que iniciaram o tratamento no estudo da Dra. Gross.
Assim, teríamos um custo de cerca de 600 mil reais a um milhão e duzentos mil reais por pessoa, por ano de tratamento. Este custo, portanto, provavelmente é muito caro para o benefício limitado que o medicamento traria para a sociedade brasileira como um todo.
Algumas análises mostraram que o selumetinibe não é custo-efetivo (ver aqui análise NICE no Reino Unido e aqui a análise CADTH no Canadá, países com saúde pública como nós), ou seja, do ponto de vista de saúde pública, não seria sustentável recomendar o medicamento. E o selumetinibe só foi aprovado nestes países porque o fabricante concordou em reduzir seu custo (o que não aconteceu aqui no Brasil).
Além disso, há uma série de procedimentos clínicos (ver no passo 8 as reavaliações periódicas) e protocolos que precisam ser seguidos para o acompanhamento dos pacientes durante seu uso, que também envolve custos financeiros.
Talvez esses custos do próprio medicamento e dos adicionais (relacionados ao protocolo de cuidados necessários e ao manejo dos eventos adversos) sejam insustentáveis para o Sistema Único de Saúde e para os Planos de Saúde.
Aqui terminamos nossos passos no Relógio de Cuidados que propomos para as pessoas que consideram a possibilidade de usarem o selumetinibe.
Nós do Centro de Referência em Neurofibromatoses do Hospital das Clínicas da Universidade Federal de Minas Gerais estamos comprometidos com nossos pacientes.
Portanto, se a ANVISA, a CONITEC e o Sistema Único de Saúde aprovarem o uso do selumetinibe para neurofibromas plexiformes sintomáticos e inoperáveis, nós faremos todo o esforço possível para criarmos as condições no Hospital das Clínicas para podermos cumprir este relógio de cuidados com cada pessoa com NF1 que nos procurar.
Belo Horizonte, 24 de dezembro de 2020 – atualizado em 20/1/2024
Nota final – Como calculamos o preço do selumetinibe?
Realizamos uma estimativa do custo do selumetinibe a partir de dados de outros países, pois ainda não temos seu preço fixado no Brasil.
- Considerando que a dose recomendada do medicamento foi de 25 mg por metro quadrado de superfície corporal duas vezes por dia, em ciclos de 28 dias;
- Considerando que a idade mediana das crianças incluídas foi de 10,2 anos; portanto, pode ser estimada uma superfície corporal mediana inicial de 1,171 m2 (meninos), crescendo até o final do estudo para 1,43 m2 e podendo chegar numa pessoa de 20 anos a 1,87 m2;
- Considerando que o preço mais baixo (em busca online, em sites dos EUA) foi de cerca de US$ 8.680,00 por caixa com 120 comprimidos de 10 mg = US$ 7,23 dólares por mg;
- Considerando que a conversão do dólar para reais seria de 5,4;
- Podemos estimar o custo mediano mensal do medicamento (ver tabela abaixo), que pode variar de cerca de 50 mil reais (para uma criança de 10 anos) a cerca de 100 mil reais (para um adulto de 20 anos) por mês.
Ver abaixo planilha com cálculo do custo do selumetinibe em termos médios.
| Idade |
área SC
a partir de peso e altura (DuBois) |
dose/m2 |
dose diária mg |
dias de uso |
preço U$/mg |
valor U$ |
custo mensal
R$ |
custo anual
R$ |
| menina 10,2 anos (início) |
0,914 |
25 |
45,7 |
28 |
7,23 |
5,4 |
49.969,13 |
599.629,62 |
| menino 10,2 anos (inicio) |
0,932 |
25 |
46,6 |
28 |
7,23 |
5,4 |
50.962,90 |
611.554,79 |
| menina (13,4 anos) final |
1,469 |
25 |
73,4 |
28 |
7,23 |
5,4 |
80.272,51 |
963.270,15 |
| menino (13,4 anos) final |
1,475 |
25 |
73,8 |
28 |
7,23 |
5,4 |
80.638,22 |
967.658,63 |
| adulto feminino |
1,621 |
25 |
81,0 |
28 |
7,23 |
5,4 |
88.576,67 |
1.062.919,99 |
| adulto masculino |
1,875 |
25 |
93,7 |
28 |
7,23 |
5,4 |
102.468,84 |
1.229.626,12 |
Qual seria o impacto deste medicamento sobre o Sistema Único de Saúde?
- Considerando que dentre a população brasileira estimada com NF1 (cerca de 80 mil pessoas) haveria um grupo de 10% da população com plexiformes sintomáticos e inoperáveis (ou seja, 8 mil pessoas potencialmente usuárias do selumetinibe);
- Considerando que o custo médio mensal seria de cerca de 80 mil reais (entre 50 e 100 mil reais como calculado acima);
- Teríamos o custo estimado para o SUS de 640 milhões de reais por mês.
- Considerando que o tempo mediano de tratamento para metade dos voluntários que sustentaram o efeito do medicamento foi de 3,2 anos no estudo da Dra. Gross e col. 2020;
- Teríamos o custo total de cerca de 11 bilhões de reais para o tratamento de metade das pessoas com plexiformes sintomáticos e inoperáveis por três anos.