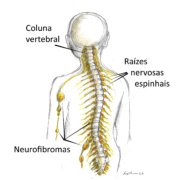
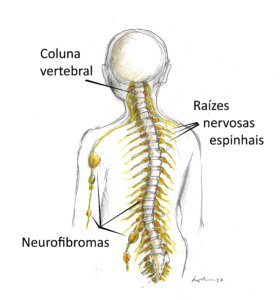
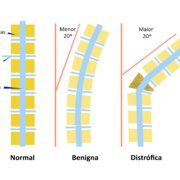
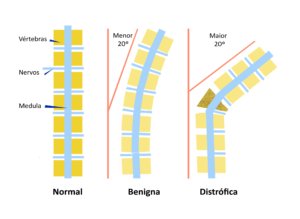
G.M.S.O. de Florianópolis pergunta: “Tenho NF1 e entrei na menopausa, estou com muito calorão, depressão e outros problemas. Já retirei o útero por causa de miomas. A médica receitou um medicamento à base de estrógeno. Ouvi dizer que hormônios aumentam os neurofibromas. Posso usar?”
Agradecemos sua pergunta, pois ela pode ser útil a outras mulheres com NF1.
O tratamento atual mais eficaz para os sintomas da menopausa é a terapia de reposição hormonal com estrogênio isolado ou combinado com progesterona. Além disso outros tratamentos não hormonais podem ser úteis (ver aqui).
Infelizmente, ainda não conhecemos estudos científicos específicos para mulheres com NF1 que tenham analisado o efeito da terapia de reposição hormonal sobre o crescimento dos neurofibromas.
Apesar da falta de estudos sobre a menopausa especificamente, algumas informações sugerem que os níveis dos hormônios femininos parecem não afetar o crescimento dos neurofibromas.
Por exemplo, as alterações hormonais da puberdade não aceleraram o crescimento do neurofibroma plexiforme em um estudo prospectivo (ver aqui).
Outro estudo baseado em ressonância magnética não encontrou diferença significativa nas taxas de crescimento de neurofibromas plexiformes ou cutâneos em gestantes com NF1 (ver aqui).
E a progesterona?
Por outro lado, algumas pesquisas sugerem um risco com medicamentos contendo progesterona (ver abaixo as explicações científicas).
Um estudo com 59 mulheres com NF1 que utilizavam contraceptivos hormonais (ver aqui) revelou que as preparações orais de estrogênio-progesterona ou de progesterona pura não estimularam o crescimento de neurofibromas na grande maioria (91%) dos casos. No entanto, duas pacientes que receberam contraceptivos de depósito com altas doses de progesterona sintética relataram crescimento tumoral significativo.
Por isso, o guia da associação norte-americana de genética clínica informa que os contraceptivos orais não parecem afetar o crescimento dos neurofibromas, mas a progesterona em altas doses exige cautela (ver aqui).
Em conclusão
A terapia de reposição hormonal (TRH) padrão na menopausa (que utiliza doses hormonais mais baixas do que os contraceptivos orais ou injetáveis durante a gravidez) provavelmente apresenta um risco teórico baixo, mas não desprezível, de estimular o crescimento de neurofibromas, particularmente por meio da progesterona.
Se a terapia hormonal for considerada, utilizar estrogênio transdérmico em baixa dose (com a menor dose eficaz de progesterona para proteção endometrial, caso o útero esteja intacto) pode ser uma abordagem razoável, embora seja uma extrapolação e não baseada em evidências.
Devem ser discutidas alternativas não hormonais, como medicamentos como a gabapentina e terapia cognitivo-comportamental.
Para a síndrome geniturinária da menopausa, pode-se considerar o uso de estrogênio vaginal em baixa dose ou prasterona intravaginal, visto que a absorção sistêmica é mínima.
É aconselhável um acompanhamento clínico rigoroso da carga de neurofibroma (incluindo atenção ao crescimento rápido ou ao surgimento de novos sintomas) caso seja iniciada a terapia hormonal sistêmica.
No seu caso, cara G., que está usando apenas estrogênio para tratamento da menopausa, os conhecimentos atuais sugerem que não há risco de aumento dos neurofibromas.
Explicações científicas para as diferenças entre estrógeno e progesterona na NF1
Aproximadamente 75% dos neurofibromas expressam receptores de progesterona, enquanto apenas cerca de 5% expressam receptores de estrogênio clássicos. No entanto, 100% dos neurofibromas cutâneos expressam o receptor de estrogênio 1 acoplado à proteína G não clássica (GPER-1), e neurofibromas maiores apresentam maior expressão tanto de PR quanto de GPER-1 (trabalho da pesquisadora brasileira Karin Cunha com a participação do Dr. Riccardi – ver aqui).
In vitro, a progesterona aumenta a proliferação de células de Schwann derivadas de neurofibromas — particularmente aquelas com inativação bialélica de NF1 (NF1−/−), enquanto as células de Schwann normais não são afetadas.
Da mesma forma, o estradiol aumenta a proliferação de células de Schwann NF1−/− em até 99% in vitro.
Em um modelo de xenotransplante, o estrogênio aumentou o crescimento de todos os três xenotransplantes de tumor maligno da bainha do nervo periférico testados e de alguns xenotransplantes de neurofibroma dérmico, embora as respostas tenham sido heterogêneas entre os diferentes tipos de tumor.
Em conclusão, precisamos de mais estudos clínicos que verifiquem o efeito real da reposição hormonal sobre o crescimento dos neurofibromas.
Referências (clique nos links para ver os artigos em inglês)
8 . Efeito da gravidez na dinâmica de crescimento de neurofibromas na neurofibromatose tipo 1. (2020)
9 . Puberdade e crescimento tumoral de neurofibroma plexiforme em pacientes com neurofibromatose tipo I. (2014)
11 . Como lidar com os sintomas da menopausa: perguntas e respostas frequentes. (2023)
12 . Tratamento dos sintomas da menopausa quando a terapia hormonal é contraindicada. (2025)