Tenho grande satisfação em publicar mais um dos capítulos escritos para a Edição Comemorativa dos 20 anos do CRNF, a ser lançada em dezembro de 2024, com o texto da psicóloga Alessandra Cerello, profissional experiente e uma das cientistas pioneiras no atendimento psicoterápico de pessoas com NF1. Muito obrigado, em nome de toda a equipe do CRNF.
Dr. Lor
Alessandra Craig Cerello
Psicóloga e Mestre
pelo Programa de Pós Graduação
em Saúde do Adulto da FM da UFMG
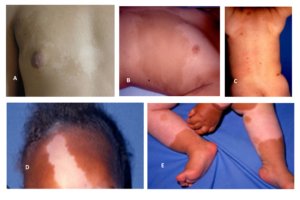
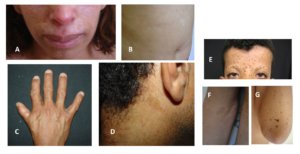
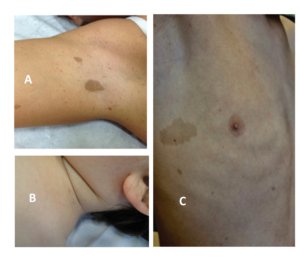
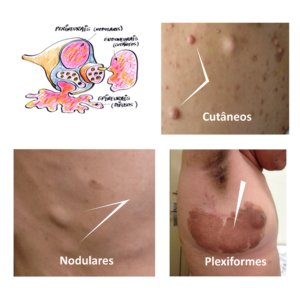
Nos capítulos já publicados, foi discutido como a NF1 afeta física e cognitivamente, por acometer diversos sistemas do organismo: nervoso, musculoesquelético, cardiovascular e endócrino. Neste capítulo, veremos como essas alterações podem afetar as pessoas com NF1 e seus familiares no que se refere aos aspectos psicoemocionais.
O funcionamento psicológico do ser humano é multideterminado, sendo influenciado por fatores intrínsecos genéticos (biológicos) e fatores extrínsecos ambientais atrelados ao contexto histórico, que são aprendidos socialmente. Nos últimos 30 anos, diversos autores vêm buscando a interface entre a NF1 e aspectos psíquicos 1,2,3,4 e efeitos na qualidade de vida 5,6.
Desde o nascimento, o ser humano é incluído em grupos sociais: a família, inicialmente, posteriormente escola, comunidade, grupo do trabalho e outros. A partir da interação com o outro, as percepções experimentadas pelos sentidos dos objetos do mundo e de si mesmo são nomeadas e, assim, progressivamente diferenciadas e classificadas.
Essas informações vão se somando, e o indivíduo vai absorvendo e ajustando como as características atribuídas a ele se assemelham ou se diferenciam das outras pessoas, para que a construção daquilo que é conhecido por “eu”, por “mim”, por “mim mesmo” seja formada 7.
Por ser um processo construído nas e pelas relações ao longo da vida, essas informações assimiladas não são nem apenas passivas e nem puramente objetivas, mas contém valores e outros aspectos subjetivos dos outros. Segundo Mead (2018), a formação da identidade é um processo de interiorização do julgamento do outro 8.
Como isso, seus derivados – o autoconceito e a autoestima – também adquirem valorização ou desvalorização, seja geral ou específica para algumas habilidades ou pela falta delas a partir das experiências vividas com essas interações.
A avaliação do autoconceito nos domínios geral e habilidades específicas demonstrou pior escore no domínio de habilidades físicas em crianças com NF1 9,10 e competência social, com aumento das chances de problemas sociais e emocionais 9. Para adolescentes, o autoconceito também foi pior em habilidades físicas, matemática e autoestima geral, tanto para os grupos com NF1 apenas e nos grupos com NF1 associada a dificuldades de aprendizagem e TDAH 10.
Pior autoestima nas pessoas com NF1 em relação a pessoas sem NF1 e irmãos sem a doença 11,12 foi descrita e associada a dificuldade de aprendizagem 10. Apesar disso, autoestima elevada em alguns participantes foi observada 12,13, e esteve associada a ter amigos com NF1, frequentar grupos de apoio para pessoas com NF1 e ter recebido orientação genética 12.
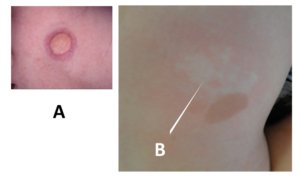
A preocupação com as alterações estéticas pode ser intensificada em algumas situações, como na puberdade, período em que as pessoas jovens estão mais preocupadas com seu corpo e quando os neurofibromas cutâneos costumam aumentar e ficar mais visíveis 1,10. Pode também ser diferente de acordo com algumas culturas, como caso descrito por Rozario (2007) de uma mulher indiana em que os impactos sociais da NF1 tiveram efeitos amplificados em suas vivências incluindo na de escolha de parceiros e casamento na vida adulta 14.
As vivências de estigmatização são uma forma de discriminação na qual a falta de aceitação social do indivíduo por uma comunidade ou cultura implica que o outro enxerga a diferença como uma inferiorização 15. A NF1 pode aumentar a chance de que isso ocorra tanto pela questão estética das alterações físicas, como pela redução da funcionalidade no que diz respeito a alterações cognitivas e de linguagem, impactando na autoestima.
Um artigo de Koerling (2020) traz um relato que ilustra outra situação comum a pessoas com NF1: a dificuldades para se ter amigos 16. Após já ter sido examinado por quatro estudantes de medicina em um hospital-escola, David respondeu a uma estudante que identificou que ele poderia ter NF1:
“Ou como eu chamo, Sem Amigos 1” Koerling (2020) (‘or as I call it, No Friends 1’ – pág 2) 16.
Hummelvoll & Antonsen (2013) avaliaram que em geral os adultos consideraram ter amigos e que muitos deles descreveram que a questão das amizades melhorou na vida adulta em relação à infância, incluindo a presença de amigos com NF1 17.
O retraimento social descrito na NF1 2,14,17 ainda não está completamente explicado na literatura. Não se sabe se resulta exclusivamente das vivências de estigmatização e bullying ou se alguma alteração na expressão genética interfere 3, por exemplo, a partir de problemas cognitivos gerais derivados de dificuldade na velocidade do processamento de informações e déficit do controle cognitivo, resultando em pior performance 4.
A influência em aspectos psicoemocionais, de forma geral, não aparentam estar necessariamente associados com a gravidade física da doença 5,6,9,10,11,17,19,20 exceto em quando a gravidade foi relacionada ao funcionamento neurocognitivo 4,18.
Já quando a avaliação da doença é comparada com a visibilidade dos sintomas, os dados são mais concordantes em apontar associações 1,2,6,17,19. Ainda assim, há discordâncias. Enquanto para Caballo et al. (2023) a maior visibilidade dos sintomas foi associada a ansiedade severa 21, outros resultados não associaram os sintomas emocionais à visibilidade do sintoma, mas a dificuldades de aprendizagem 12,18.
Em estudo qualitativo realizado com perguntas semiestruturadas realizado no Centro de Referência em Neurofibromatose-MG (CRNF-MG) no Brasil, alguns entrevistados descreveram o enfrentamento da doença como sendo “normal, natural”, enquanto outros focaram em sentimentos negativos de medo e consequências negativas da doença por limitações e constrangimentos sociais, reforçando que a experiência com NF1 varia de sujeito para sujeito 22.
Sintomas psicológicos classificados como internalizantes (que são aqueles nos quais a reação é voltada da pessoa para ela mesma) como ansiedade, depressão e retraimento social 5,9,18,19 foram descritos com mais frequência e concordância entre os autores, que sintomas classificados como externalizantes (aqueles em que a reação é direcionada principalmente a uma ação que repercute no ambiente de um indivíduo), como impulsividade e agressividade 18 que foram menos presentes ou presente apenas em idades mais precoces 4.
A depressão e a ansiedade são condições presentes na população em geral. O aumento dos transtornos ansiosos e depressivos vem sendo associado a questões contemporâneas, como o estilo de vida atual da sociedade, centrada em alta performance, em padrões estéticos e comportamentais, nos quais há valorização da pessoa multitarefas, extrovertida e comunicativa. Na NF1, a presença de doenças psiquiátricas, como depressão, ansiedade e estresse foi associada a reações subjetivas diante das desfigurações decorrentes das alterações estéticas, vivências de estigmatização e alterações no estilo de vida 19.
Enquanto a ansiedade tem se mostrado como um achado concordante entre os autores, os dados relativos à depressão apresentaram menos concordância 4,9,18,23. Possíveis explicações apresentadas são diferentes delineamentos dos estudos, como faixa etária estudada e critérios para a mensuração dos dados. Por exemplo, há diferenças entre as respostas quando as escalas de avaliação são preenchidas pelos profissionais, pelos familiares, pelos professores ou pela própria pessoa com NF1 18,24,25.
Uma alteração mais branda do humor, a distimia, foi avaliada como diagnóstico psiquiátrico mais comum em avaliação longitudinal de 12 anos 13, que também indicou que vivências de estigmatização podem estar envolvidas. Sinais mais graves de depressão com ocorrências de ideações de autoextermínio (IAE) foram descritas em 16% das crianças com NF1 em comparação com 6% dos irmãos sem a doença 9 e em 45% de entrevistados adultos com NF1 contra 10% dos controles sem NF1 26.
Há ainda muito desconhecimento sobre a NF1, o que dificulta a identificação de sinais e sintomas por familiares e o diagnóstico da NF1 por profissionais 22,27. Essa falta de informações e referências sobre a NF1 para a sociedade leva a uma situação de invisibilidade social da doença apesar da visibilidade dos sintomas físicos e comportamentais 22.
Alguns centros de tratamento têm utilizado mídias sociais como instrumento de divulgação de informações técnicas e mesmo como meio para favorecer o encontro de pessoas com NF1 e familiares, como a Associação Mineira de Apoio às Pessoas com Neurofibromatoses (AMANF). Isso é importante, sobretudo no que se refere à ampliação do acesso a informações e construção de redes de suporte e troca de experiência.
Se por um lado a tecnologia pode aproximar as pessoas e há ganhos válidos com isso (teleconsultas, facilitação do acesso de pessoas com menor mobilidade etc.), algumas pessoas que não se sentem capazes de se utilizar dela podem sentir o efeito contrário, aumentando o sentimento de auto culpabilização e solidão para quem já se sentia à margem. Além disso, a exposição maior pode ser mais um canal para que se experimente bullying, o cyberbullying 21.
Em resumo, apesar das diferenças individuais, em geral o impacto psicológico da NF1 para as pessoas com NF1 é:
- Avaliado de forma diferente por profissionais, familiares ou a própria pessoa;
- Menos afetado pela gravidade da doença do que pelas dificuldades de aprendizagem, pela visibilidade dos sintomas os constrangimentos sociais vividos em situações de estigmatização, discriminação e bullyng;
- Diferente ao longo das etapas da vida (infância, adolescência, vida adulta);
- Manifestado mais comumente por sintomas psicológicos internalizantes, em destaque para a ansiedade, do que sintomas externalizantes.
Propostas
Diante dos impactos psicossociais da NF1, Johnson et al. (1999) propõe quatro ações 9:
1 – orientar os pais de crianças com NF1 quanto risco aumentado de problemas sociais e afetivos;
2 – avaliar periódica das crianças com NF1 e tratamento dos problemas de linguagem, motores e cognitivos, visando à possível redução de problemas sociais e emocionais;
3 – encaminhar para avaliação psiquiátrica e/ou psicológica padronizada nos casos de problemas sociais e afetivos;
4 – ampliar as possibilidades de intervenção terapêutica pelos centros de tratamento, buscando prevenir e tratar esses problemas.
Tendo em vista que os familiares também estão sob estresse e respondem emocionalmente às questões atreladas à NF1 17,27 faz-se importante um espaço de escuta e acolhimento para eles. Além disso, um suporte familiar adequado favorece que o apoio social para a pessoa com NF1 seja de melhor qualidade, possibilitando efeitos protetores na qualidade de vida das crianças e adolescentes com NF1 5 e mesmo de adultos 23.
A imprevisibilidade do desenvolvimento da doença é um fator que a torna difícil para se compreender e para se enfrentar 1 além de mais ansiogênico 2. Por essa razão, o olhar dos profissionais é fundamental na identificação dos sinais psicoemocionais, para orientação e encaminhamentos adequados. O relato de David 16 relembra de uma ação simples, mas nem sempre bem utilizada. Uma pergunta cotidiana: “como você está se sentindo?” acompanhada por uma abertura sincera pelo profissional a uma escuta atenta da pessoa é indispensável na identificação precoce ou mesmo a tempo de fatores que possam sugerir sofrimento psíquico, incluindo aqueles com maior intensidade. Essas respostas podem incluir as IAE. Nesse caso, o profissional deve estar preparado e conhecer sobre a rede de atendimento psicossocial local para referenciar a pessoa ao cuidado necessário.
Acerca das IAE alguns mitos precisam ser desfeitos, como orienta a Cartilha de Prevenção ao Suicídio do Ministério da Saúde: falar sobre morrer não incentiva um ato de tentativa de autoextermínio, ao contrário, pode auxiliar a apaziguar a pessoa com uma escuta acolhedora e mesmo prevenir o ato 28.
Referências
1- Mouridsen SE, Sorensen SA. Psychological aspects of von Recklinghausen neurofibromatosis (NFl). J Med Genet. 1995; 32:921-4.
2- Ablon J. Living with genetic disorder: The impact of Neurofibromatosis 1. Auburn House, Westport, CT. 1999
3- Martin S, Wolters P, Baldwin A, Gillespie A, Dombi E, Walker K, Widemann B. Social-emotional functioning of children and adolescents with neurofibromatosis type 1 and plexiform neurofibromas: Relationships with cognitive, disease, and environmental variables. Journal of Pediatric Psychology. 2012; 37(7), 713–724.
4- Huijbregts SC, Sonneville LM. Does cognitive impairment explain behavioral and social problems of children with neurofibromatosis type 1? Behav Genet. 2011; 41:430–436.
5- Graf A, Landolt MA, Mori AC, Boltshauser E. Quality of life and psychological adjustment in children and adolescents with neurofibromatosis type 1. The Journal of Pediatrics. 2006; 149(3), 348–353.
6- Page PZ, Page GP, Ecosse E, Korf BR, Leplege A, Wolkenstein P. Impact of neurofibromatosis 1 on Quality of Life: A cross-sectional study of 176 American cases. American Journal of Medical Genetics Part A. 2006; 140A(18), 1893–1898.
7- Papalia DE, Olds SW, Feldman RD. Desenvolvimento humano. Porto Alegre: Artmed, 2000. 684p.
8- Mead GH. Mente, self e sociedade: edição definitiva. Petrópolis: Vozes, 2021. 424p
9- Johnson NS, Saal HM, Lovell AM, Schorry EK. Social and emotional
problems in children with neurofibromatosis type 1: Evidence and proposed interventions. J Pediatr. 1999; 134:767–772.
10- Barton B, North K. The self-concept of children and adolescents with neurofibromatosis type 1. Child Care Health Dev. 2007; 33:401–408.
11- Wang D, Smith K, Esparza S, Leigh F, Muzikansky A, Park E, et al. Emotional functioning of patients with neurofibromatosis tumor suppressor syndrome. Genetics in Medicine. 2012; 14(12), 977–982.
12- Rosnau K, Hashmi SS, Northrup H, Slopis J, Noblin S, Ashfaq M. Knowledge and Self-Esteem of Individuals with Neurofibromatosis Type 1 (NF1). Journal of Genetic Counseling. 2016; 26(3), 620–627.
13- Zöller ME, Rembeck B. A psychiatric 12-year follow-up of adult patients with
neurofibromatosis type 1. J Psychiatr Res. 1999; 33: 63–68.
14- Rozario S. Growing Up and Living with Neurofibromatosis1 (NF1): A British Bangladeshi Case-study. Journal of Genetic Counseling. 2007; 16(5), 551–559.
15- GOFFMAN E. Estigma: Notas sobre a Manipulação da Identidade Deteriorada. Quarta Edição. LTC. Rio de Janeiro, 2008. 158p.
16- Koerling AL. No friends 1. Orphanet Journal of Rare Diseases. 2020; 15(1).
17- Hummelvoll G, Antonsen KM. Young adults’ experience of living with neurofibromatosis type 1. J. Genet. Couns. 2013; 22, 188–199.
18- Noll RB, Reiter-Purtill J, Moore BD, Schorry EK, Lovell AM, Vannatta K, Gerhardt CA. Social, emotional, and behavioral functioning of children with NF1. Am J Med Genet Part A. 2007; 143:2261–2273.
19- Wolkenstein P, Zeller J, Revuz J, Ecosse E, Leplege A. Visibility of
neurofibromatosis 1 and psychiatric morbidity. Arch Dermatol. 2003; 139: 103–104.
20- Sebold CD, Lovell A, Hopkin R, Noll R, Schorry E. Perception of disease severity in adolescents diagnosed with neurofibromatosis type 1. J. Adolesc. Health. 2004; 35, 297–302.
21- Cavallo ND, Maggi G, Ferraiuolo F, Sorrentino A, Perrotta S, Carotenuto M, Santangelo G, Santoro C. Neuropsychiatric Manifestations, Reduced Self-Esteem and Poor Quality of Life in Children and Adolescents with Neurofibromatosis Type 1 (NF1): The Impact of Symptom Visibility and Bullying Behavior. Children. 2023; 10, 330.
22- Cerello AC, Gianorlodi-Nascimento IF, Moreira AH, Rocha VS, Ribeiro LM, Rezende NA. Representações sociais de pacientes e familiares sobre neurofibromatose tipo 1. Ciênc. saúde coletiva. 2013; 18 (8) Ago.
23- Buono FD, Sprong ME, Paul E, Martin S, Larkin K, Garakani A. The mediating effects of quality of life, depression, and generalized anxiety on perceived barriers to employment success for people diagnosed with Neurofibromatosis Type 1. Orphanet J. Rare Dis. 2021; 16, 234.
24- Pasini A, Lo-Castro A, Di Carlo L, Pitzianti M, Siracusano M, Rosa C, Galasso C. Detecting anxiety symptoms in children and youths with neurofibromatosis type I. American Journal of Medical Genetics, Part B: Neuropsychiatric Genetics. 2012; 159B(7), 869–873.
25- Cipolletta S, Spina G, Spoto A. Psychosocial functioning, self-image, and quality of life in children and adolescents with neurofibromatosis type 1. Child: Care, Health and Development. 2018; 44(2), 260–268.
26- Berardelli I, Maraone A, Belvisi D, Pasquini M, Giustini S, Miraglia E, Iacovino C, Pompili M, Frascarelli M, Fabbrini G. The importance of suicide risk assessment in patients affected by neurofibromatosis. International Journal of Psychiatry in Clinical Practice. 2021; 25(4), 350–355.
27- Quintais ALS. Neurofibromatose Tipo 1: Principais Preocupações de Doentes e Cuidadores de Doentes. (Dissertação) Mestrado Integrado em Psicologia. Faculdade de Psicologia e de Ciências da Educação da Universidade de Lisboa. Luísa Barros (orientadora). 2008. 56p.
28- Brasil. Cartilha de Prevenção ao Suicídio. Sem data. Disponível em: https://www.gov.br/mre/pt-br/consulado-miami/assistencia-a-brasileiros/cartilha-de-prevencao-ao-suicidio