Tratamento da dor nas pessoas com NF
Informações atualizadas pelos médicos Renato Viana e Luiz Oswaldo Carneiro Rodrigues para orientação do tratamento da dor em pessoas com Neurofibromatoses (NF).
Estas orientações estão apresentadas em duas partes:
- Pessoas com NF e suas famílias
- Proffissionais da saúde
Em ambas as partes, sempre que você clicar nas letras em vermelho você poderá obter mais informações sobre o assunto e/ou referências científicas.
Parte A – Para pessoas com NF e suas famílias
As pessoas com qualquer uma das doenças genéticas conhecidas anteriormente como neurofibromatoses (NF) podem sentir dor, às vezes por longos períodos (ver aqui os novos nomes para as NF a partir de 2022).
Mais da metade das pessoas com Neurofibromatose do tipo 1 (NF1) se queixa de algum tipo de dor.
Pessoas com Schwannomatose relacionada ao gene NF2 (SRNF2) (antes chamada de NF2) algumas vezes sentem dor.
Pessoas com Schwannomatoses relacionadas aos genes SMRCB1 e LZTR1 (antes chamadas apenas de Schwannomatose) apresentam dor como a principal complicação da doença.
Para tratarmos corretamente as dores destas pessoas, precisamos compreender o que é a dor e como nosso cérebro percebe o que é doloroso.
O que é a dor?
Segundo a última convenção internacional, a dor é uma experiência sensitiva e emocional desagradável associada, ou semelhante àquela associada, a uma lesão verdadeira ou potencial dos tecidos.
Ou seja, a dor é uma sensação ruim e carregada de emoção que é percebida por uma pessoa como se uma certa parte do seu corpo tenha sido, esteja sendo ou possa vir a ser machucada.
A dor é uma percepção individual, ou seja, somente quem a sente pode dizer sobre sua intensidade e como ela afeta a sua qualidade de vida. Ninguém é capaz de medir a dor e o sofrimento da outra pessoa, nem mesmo profissionais de saúde.
Para saber mais sobre este aspecto pessoal e intransferível da dor, veja o depoimento da associada da AMANF, engenheira e professora Ana de Oliveira Rodrigues em seu post: “Mas isso não dói” (clique no título).
Além de ser individual, a dor pode ser aguda, ou seja, de início recente, ou crônica, quando a sua duração ultrapassa mais de 3 meses.
A dor pode ter uma causa simples e evidente, por exemplo, um trauma, ou ter causas complexas e de difícil diagnóstico.
Quando a dor surge por causa da lesão de um órgão, de um tecido ou parte do corpo, ela é chamada de nociceptiva (essa palavra quer dizer percepção da lesão).
Quando a dor surge por causa de alterações no funcionamento do próprio sistema nervoso, ela é chamada de neuropática (a palavra quer dizer originada de um problema neurológico).
Às vezes, a dor pode ser mista, quer dizer, causada tanto por lesões nos tecidos quanto por mal funcionamento do sistema nervoso. Ver abaixo os tipos de dor definidas internacionalmente.
É preciso conhecer a dor para que possa ser tratada de forma eficiente. Por isso, é fundamental profissionais da saúde utilizarem um sistema de diagnóstico e avaliação da intensidade da dor, que possa expressar o sentimento da pessoa que sofre com ela.
Adiante mostraremos os questionários e métodos científicos que podem ser usados para esta finalidade.
Antes, vamos rever brevemente como nós percebemos a dor
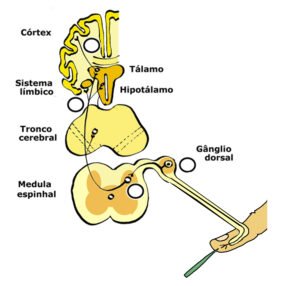
A Figura 1 ilustra como a dor é percebida. Imagine que um alfinete furou a pele e atingiu o ramo de um nervo especializado em perceber a dor (neurônio do nível 1).
O sinal elétrico provocado pelo alfinete percorre a fibra nervosa (como se fosse um fio) até a medula, onde estimula outro neurônio sensitivo (neurônio do nível 2).
O neurônio da medula repassa novo sinal para outros neurônios (do nível 3), com cópias desse estímulo para outras estruturas do cérebro (neurônios do nível 4), onde a pessoa toma consciência da picada do alfinete e localiza exatamente onde ela aconteceu.
Em cada uma dessas etapas, do neurônio 1 ao neurônio 4, diversos fatores podem modificar a transmissão da dor até o cérebro e a mesma picada de alfinete pode ser percebida de formas diferentes, dependendo das condições em que estão as comunicações entre os diversos níveis.
Por exemplo, o estado emocional pode aumentar (na ansiedade, por exemplo) ou diminuir (na meditação, por exemplo) a percepção da dor.
Os medicamentos anestésicos e analgésicos funcionam interrompendo ou dificultando a passagem do estímulo desde a picada do alfinete até a consciência da pessoa e modulando os neurônios inibidores e excitadores.
Esta variação da percepção da dor acontece porque existem outros neurônios e substâncias que modulam (inibem ou excitam) os neurônios envolvidos em cada etapa da transmissão da dor da periferia até o cérebro.
Quem desejar mais detalhes destas etapas, ver outra Figura e sua explicação no final deste texto.
Quais os tipos de dor?
Existem quatro tipos de dor:
- Provocadas por uma lesão ou pelo risco de lesão em tecidos corporais, por exemplo, um corte inflamado ou infeccionado na pele.
- Provocada por uma lesão ou disfunção do próprio sistema nervoso. (Esse tipo é a dor Neuropática, que nos interessa mais).
- Provocada por alterações no processamento da dor no próprio cérebro, mas sem lesão verdadeira nos tecidos.
- Provocada por combinações de lesões nos tecidos e alterações no sistema nervoso.
As pessoas com neurofibromatoses podem apresentar qualquer um dos tipos de dor e o seu tratamento é semelhante ao das pessoas sem NF. No entanto, considerando que muitas pessoas com NF apresentam dor crônica e dor neuropática, vamos nos aprofundar neste tipo de dor.
A dor neuropática é uma doença?
Sim, a dor neuropática é considerada uma doença em si. A dor neuropática é causada por lesões ou alterações na função dos próprios nervos e do sistema nervoso central.
A dor neuropática pode ser percebida como dor, queimação, picada, choque, beliscão, calor e frio em ondas que vêm e vão, às vezes relacionadas com fatores ambientais, emocionais e físicos.
Outras vezes, a dor neuropática pode surgir sem qualquer estímulo evidente ou até mesmo num membro que já foi amputado, como a chamada dor fantasma.
O primeiro passo para tratar, é quantificar a dor
Geralmente utilizamos uma escala visual, uma régua marcada de 1 a dez, sendo 0 nenhuma dor e 10 a maior dor que a pessoa já sentiu. Pedimos para a pessoa apontar na escala qual a intensidade da dor que ela está sentindo ou sentiu.
A nota deve ser registrada em cada reavaliação.
O segundo passo é definir se a dor é do tipo neuropática.
Um questionário bastante simples pode ser usado, basta responder sim ou não.
Cada resposta positiva representa 1 ponto. Some os pontos.
Sensação de dor:
- Em queimação
- Frio doloroso
- Como choque elétrico
Sintomas na mesma área da dor:
- Adormecimento
- Formigamento
- Alfinetadas
- Coceira
Exame físico:
- Menor sensibilidade ao toque?
- Menor sensibilidade à ponta de agulha?
- Dor provocada ou aumentada pelo atrito?
Resultado da soma: maior do que 3 pontos sugere dor neuropática
O terceiro passo é procurar uma causa para a dor neuropática.
Exemplos de causas da dor neuropática:
- Lesão crônica envolvendo o nervo (inflamação, compressão, corte e cicatrização) produz substâncias inflamatórias que estimulam as terminações nervosas e fazem com que elas enviem estímulos exagerados ao cérebro. Por isso, os antinflamatórios, o gelo e alguns analgésicos atuam neste ponto, reduzindo o processo inflamatório e aliviando a dor.
- Compressão mecânica, por exemplo, um neurofibroma comprimindo o nervo, causando irritação ou mesmo amputando o nervo. Por isso, a remoção cirúrgica de neurofibromas compressivos pode aliviar algumas formas de dor neuropática.
- Destruição ou o corte do nervo podem causar cicatrização anormal, que produz uma espécie de tumor na ponta do nervo cortado, que chamamos de neuroma. Esse enovelado irregular e disfuncional de fibras nervosas pode produzir estímulos excessivos, que são percebidos como dor fantasma, como acontece nas amputações.
- Dor não tratada por muito tempo pode alterar a expressão genética de proteínas que controlam a dor (como a neurofibromina, inclusive) aumentando a sensibilidade dolorosa da pessoa. Por isso, sinais de compressão nervosa devem ser tratados com rapidez. Uma dor não tratada hoje pode ser uma dor aumentada amanhã.
- Problemas na medula espinhal podem alterar a sensibilidade dolorosa. A noradrenalina é importante nesse processo e por isso observamos aumento da sensibilidade dolorosa durante situações de estresse.
- Modificações no sistema nervoso central podem aumentar a sensibilidade dolorosa.
- Fatores emocionais e pelo estado de humor afetam a sensibilidade à dor.
- Experiência, história de vida e cultura afetam a percepção da dor. A memória, o conhecimento e o aprendizado da dor participam da regulação de como percebemos a dor e o medo que ela nos causa. Também sabemos que a depressão e a ansiedade podem aumentar a sensação de dor. Por isso, antidepressivos e ansiolíticos podem ajudar a controlar a dor, inclusive nas neurofibromatoses.
- As características genéticas afetam a percepção da dor. Boa parte (40%) da sensibilidade à dor pode ser atribuída a fatores genéticos. Neste sentido, parece que as pessoas com NF1 têm a sensibilidade dolorosa aumentada de um modo geral.
- Outras causas – é possível haver outros mecanismos de dor nas neurofibromatoses que desconhecemos por enquanto.
Em resumo, dores de diferentes intensidades e causas podem estar agindo ao mesmo tempo numa pessoa com neurofibromatose e por isso o tratamento da dor crônica e da dor neuropática geralmente é complexo e multidisciplinar.
Tratamentos para dor crônica (ESPECIALMENTE NEUROPÁTICA)
O primeiro passo para o tratamento adequado é diagnosticar e quantificar a dor e medir seu impacto na qualidade de vida, por meio de questionários estruturados e escalas para medir a dor e a realização de exame físico clínico por profissional experiente. Exames complementares podem ser necessários.
Está claro que o tratamento ideal será tentar remover a causa da dor.
Enquanto a causa está sendo removida (ou quando não é possível sua remoção) devemos usar outros procedimentos.
Em nosso Centro de Referência em NF do HC UFMG costumávamos recomendar a chamada escada analgésica, baseada em orientação da Organização Mundial da Saúde, que foi reavaliada em 2010.
A partir de agora, nossos profissionais da saúde utilizarão uma adaptação dos procedimentos indicados pela extensa revisão realizada por Bates e colaboradores, 2019.
Depois de diagnosticada e quantificada a dor, podem ser utilizados os passos apresentados adiante.
É muito importante saber que o tratamento da dor neuropática é quase sempre MULTIDISCIPLINAR, envolvendo profissionais da saúde que orientem para a reabilitação física, apoio psicológico, higiene do sono, exercícios físicos regulares e outras ações complementares.
Em conclusão, diante da dor, especialmente dor crônica, é fundamental procurar profissionais da saúde para a orientação adequada.
Parte B – Para profissionais da saúde
Lembre-se que ao clicar nas letras em vermelho você poderá obter mais informações sobre o assunto e/ou referências científicas.
As pessoas com qualquer uma das doenças três genéticas conhecidas anteriormente como neurofibromatoses (NF) podem sentir dor, às vezes por longos períodos (ver aqui os novos nomes para as NF a partir de 2022).
Mais da metade das pessoas com Neurofibromatose do tipo 1 (NF1) se queixa de algum tipo de dor.
Pessoas com Schwannomatose relacionada ao gene NF2 (SRNF2) (antes chamada de NF2) algumas vezes sentem dor.
Pessoas com Schwannomatoses relacionadas aos genes SMRCB1 e LZTR1 (antes chamadas apenas de Schwannomatose) apresentam dor como a principal complicação da doença.
Para tratarmos corretamente as dores destas pessoas, precisamos compreender o que é a dor e como nosso cérebro percebe o que é doloroso.
O que é a dor?
Segundo a última convenção internacional, a dor é uma experiência sensitiva e emocional desagradável associada, ou semelhante àquela associada, a uma lesão verdadeira ou potencial dos tecidos.
Ou seja, a dor é uma sensação ruim e carregada de emoção que é percebida por uma pessoa como se uma certa parte do seu corpo tenha sido, esteja sendo ou possa vir a ser machucada.
A dor é uma percepção individual, ou seja, somente quem a sente pode dizer sobre sua intensidade e como ela afeta a sua qualidade de vida. Ninguém é capaz de medir a dor e o sofrimento da outra pessoa, nem mesmo profissionais de saúde.
Para saber mais sobre este aspecto pessoal e intransferível da dor, veja o depoimento da associada da AMANF, engenheira e professora Ana de Oliveira Rodrigues em seu post: “Mas isso não dói” (clique no título).
Além de ser individual, a dor pode ser aguda, ou seja, de início recente, ou crônica, quando a sua duração ultrapassa mais de 3 meses.
A dor pode ter uma causa simples e evidente, por exemplo, um trauma, ou ter causas complexas e de difícil diagnóstico.
Quando a dor surge por causa da lesão de um órgão, de um tecido ou parte do corpo, ela é chamada de nociceptiva (essa palavra quer dizer percepção da lesão).
Quando a dor surge por causa de alterações no funcionamento do próprio sistema nervoso, ela é chamada de neuropática (a palavra quer dizer originada de um problema neurológico).
Às vezes, a dor pode ser mista, quer dizer, causada tanto por lesões nos tecidos quanto por mal funcionamento do sistema nervoso. Ver abaixo os tipos de dor definidas internacionalmente.
É preciso conhecer a dor para que possa ser tratada de forma eficiente. Por isso, é fundamental profissionais da saúde utilizarem um sistema de diagnóstico e avaliação da intensidade da dor, que possa expressar o sentimento da pessoa que sofre com ela.
Adiante mostraremos os questionários e métodos científicos que podem ser usados para esta finalidade.
Breve revisão de como nós percebemos a dor
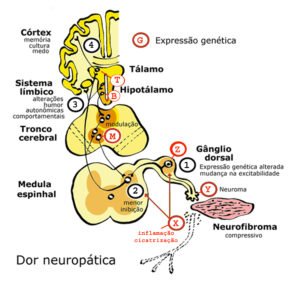
Na Figura 2 estão representados diversos fatores que influenciam a transmissão da dor, os pontos X, Y, Z, M, B e G que nos ajudarão a compreender os diferentes tipos de dor.
Começando de baixo para cima, no (ponto X na Figura 2) temos, por exemplo, uma lesão em torno do nervo (inflamação, compressão, corte e cicatrização) que produz substâncias inflamatórias que estimulam as terminações nervosas e fazem com que elas enviem estímulos exagerados ao cérebro. Por isso, os antinflamatórios, o gelo e alguns analgésicos atuam neste ponto, reduzindo o processo inflamatório e aliviando a dor.
Outras vezes a lesão é causada pela compressão mecânica, por exemplo, um neurofibroma comprimindo o nervo (ponto Y na Figura 2), causando irritação ou mesmo amputando o nervo, o que é percebido como estímulo doloroso. Por isso, a remoção cirúrgica de neurofibromas compressivos pode aliviar algumas formas de dor neuropática.
Outras vezes, a destruição ou o corte do nervo (no ponto Y) podem causar cicatrização anormal, que produz uma espécie de tumor na ponta do nervo cortado, que chamamos de neuroma. Esse enovelado irregular e disfuncional de fibras nervosas pode produzir estímulos excessivos, que são percebidos como dor fantasma, como acontece nas amputações.
No ponto Z da Figura 2, a persistência da dor não tratada pode alterar a expressão genética de proteínas que controlam a dor (como a neurofibromina, inclusive), produzindo mais receptores de glutamato e NMDA, por exemplo, e aumentando a sensibilidade dolorosa da pessoa.
Por isso, sinais de compressão nervosa devem ser tratados com rapidez. Ou seja, um pequeno estímulo que não provocaria dor, pode se transformar em dor forte por causa da sensibilidade aumentada, causada pela dor crônica não tratada. Por isso, não devemos deixar sem tratamento uma pessoa com dor. Uma dor não tratada hoje pode ser uma dor aumentada amanhã.
No ponto M da Figura 2 estão as conexões na medula espinhal entre os nervos que trazem o estímulo doloroso da periferia do corpo e os nervos que conduzem estes estímulos até os centros superiores no cérebro.
Na dor neuropática, neste ponto M pode haver menor inibição da sensibilidade dolorosa, ou seja, o filtro realizado pelos neurônios na medula estariam menos ativos, permitindo a passagem da dor com mais facilidade para os centros superiores, ou seja, sinalizando uma dor amplificada. A noradrenalina é uma das substâncias moduladoras e por isso observamos aumento da sensibilidade dolorosa durante situações de estresse.
Alguns analgésicos e a cortisona também podem agir nesse ponto M, reduzindo a dor, como, por exemplo, nos chamados bloqueios com cortisona injetada ao redor da medula.
No ponto B da Figura 2, novos filtros (modulações) dos estímulos podem ocorrer, aumentando ou diminuindo a sensibilidade dolorosa. Neste ponto, algumas drogas chamadas neurolépticas e os anticonvulsivantes podem ajudar a reduzir a passagem dos estímulos dolorosos, diminuindo a dor que chega à consciência.
No ponto T da Figura 2 a dor também é aumentada ou diminuída por fatores emocionais e pelo estado de humor. Por exemplo, uma mesma lesão física pode parecer muito mais dolorosa à noite, quando nosso estado de humor aumenta as percepções da fadiga, do cansaço e dos perigos, porque somos seres diurnos, selecionados para viver durante o dia e repousar à noite.
No cérebro existem diversas regiões onde armazenamos informações sobre tudo aquilo que acontece conosco. Então, a memória, o conhecimento e o aprendizado da dor participam da regulação de como percebemos a dor e o medo que ela nos causa.
A dor crônica pode modificar estas estruturas por meio da plasticidade cerebral. Por isso, a psicoterapia, o acompanhamento psicológico, técnicas de meditação e controle cognitivo podem auxiliar o controle da dor neuropática nas neurofibromatoses.
Também sabemos que a depressão e a ansiedade podem aumentar a sensação de dor. Por isso, antidepressivos e ansiolíticos podem ajudar a controlar a dor, inclusive nas neurofibromatoses.
Para completar, o ponto G na Figura 2 indica a expressão genética – em todo o sistema nervoso – da herança maior ou menor sensibilidade para a dor. Parte (40%) da suscetibilidade à dor pode ser atribuída a fatores genéticos. Neste sentido, parece que a ausência da neurofibromina nas pessoas com NF1 aumenta a sensibilidade dolorosa de um modo geral.
É preciso lembrar que pode haver outros mecanismos de dor nas neurofibromatoses que desconhecemos por enquanto. Por exemplo, na NF1 não sabemos exatamente por que os neurofibromas cutâneos raramente são dolorosos, enquanto plexiformes e nodulares muitas vezes o são. Além disso, os schwannomas raramente são dolorosos na NF2, mas são muito dolorosos na Schwannomatose. E todos estes tumores se originam da mesma célula de Schwann, na bainha dos nervos periféricos!
Finalmente, sabemos que vários dos mecanismos neste esquema da Figura 2 podem estar atuando ao mesmo tempo numa pessoa com neurofibromatose e por isso o tratamento da dor neuropática geralmente é complexo e multidisciplinar.
Quais os tipos de dor?
Existem quatro tipos de dor:
- Provocadas por uma lesão ou pelo risco de lesão em tecidos corporais, por exemplo, um corte inflamado ou infeccionado na pele. Esse tipo de dor é chamado por profissionais da saúde de dor Nociceptiva.
- Provocada por uma lesão ou disfunção do próprio sistema nervoso, por exemplo, a alteração dos nervos nos pés das pessoas com diabetes. Esse tipo de dor é a dor Neuropática.
- Provocada por alterações no processamento da dor no próprio cérebro, mas sem lesão verdadeira nos tecidos onde a dor é sentida, por exemplo, na fibromialgia. Esse tipo de dor é a dor Nociplástica.
- Provocada por combinações de lesões nos tecidos e alterações no sistema nervoso. É chamada de dor Mista.
Profissionais da saúde também usam alguns outros termos técnicos para falarem da dor. Por exemplo, quando a sensibilidade está exagerada aos estímulos dolorosos, chamamos de hiperalgesia. Quando um estímulo não doloroso, o toque das mãos, por exemplo, é percebido como dor, chamamos de alodinia. Quando a dor é percebida em região diferente do local onde está ocorrendo a lesão, por exemplo, a dor do infarto agudo do miocárdio sendo percebida no braço, chamamos de dor referida.
As pessoas com neurofibromatoses podem apresentar qualquer um dos tipos de dor acima descritos e o seu tratamento é semelhante ao das pessoas sem NF. No entanto, considerando que muitas pessoas com NF apresentam dor crônica e dor neuropática, vamos nos aprofundar neste tipo de dor.
A dor neuropática é uma doença?
Sim, a dor neuropática é considerada uma doença em si. A dor neuropática é causada por lesões ou alterações na função dos próprios nervos e do sistema nervoso central.
A dor neuropática pode ser percebida como dor, queimação, picada, choque, beliscão, calor e frio em ondas que vêm e vão, às vezes relacionadas com fatores ambientais, emocionais e físicos.
Outras vezes, a dor neuropática pode surgir sem qualquer estímulo evidente ou até mesmo num membro que já foi amputado, como a chamada dor fantasma.
O primeiro passo para tratar, é quantificar a dor
Geralmente utilizamos uma escala visual, uma régua marcada de 1 a dez, sendo 0 nenhuma dor e 10 a maior dor que a pessoa já sentiu. Pedimos para a pessoa apontar na escala qual a intensidade da dor que ela está sentindo ou sentiu.
A nota deve ser registrada em cada reavaliação.
O segundo passo é definir se a dor é do tipo neuropática.
Um questionário bastante simples (chamado de DN4 – Douleur Neuropathique Quatre) pode ser utilizado (abaixo) e ele possui sensibilidade razoável (72%) e alta especificidade (97%).
Pode ser necessário esclarecer com cuidado os sintomas para as pessoas com a dor.
Basta responder sim ou não.
Cada resposta positiva representa 1 ponto. Some os pontos.
Sensação de dor:
- Em queimação
- Frio doloroso
- Como choque elétrico
Sintomas na mesma área da dor:
- Adormecimento
- Formigamento
- Alfinetadas
- Coceira
Exame físico:
- Menor sensibilidade ao toque?
- Menor sensibilidade à ponta de agulha?
- Dor provocada ou aumentada pelo atrito?
Resultado da soma: maior do que 3 pontos sugere dor neuropática
O terceiro passo é procurar uma causa para a dor neuropática.
Exemplos de causas da dor neuropática:
- Lesão crônica envolvendo o nervo (inflamação, compressão, corte e cicatrização) produz substâncias inflamatórias que estimulam as terminações nervosas e fazem com que elas enviem estímulos exagerados ao cérebro. Por isso, os antinflamatórios, o gelo e alguns analgésicos atuam neste ponto, reduzindo o processo inflamatório e aliviando a dor.
- Compressão mecânica, por exemplo, um neurofibroma comprimindo o nervo, causando irritação ou mesmo amputando o nervo. Por isso, a remoção cirúrgica de neurofibromas compressivos pode aliviar algumas formas de dor neuropática.
- Destruição ou o corte do nervo podem causar cicatrização anormal, que produz uma espécie de tumor na ponta do nervo cortado, que chamamos de neuroma. Esse enovelado irregular e disfuncional de fibras nervosas pode produzir estímulos excessivos, que são percebidos como dor fantasma, como acontece nas amputações.
- Dor não tratada por muito tempo pode alterar a expressão genética de proteínas que controlam a dor (como a neurofibromina, inclusive) aumentando a sensibilidade dolorosa da pessoa. Por isso, sinais de compressão nervosa devem ser tratados com rapidez. Uma dor não tratada hoje pode ser uma dor aumentada amanhã.
- Problemas na medula espinhal podem alterar a sensibilidade dolorosa. A noradrenalina é importante nesse processo e por isso observamos aumento da sensibilidade dolorosa durante situações de estresse. Alguns analgésicos e a cortisona também podem ser úteis, reduzindo a dor, como, por exemplo, nos chamados bloqueios com cortisona injetada ao redor da medula.
- Modificações no sistema nervoso central podem aumentar a sensibilidade dolorosa, por isso algumas drogas chamadas neurolépticas e os anticonvulsivantes podem ajudar a reduzir a passagem dos estímulos dolorosos, diminuindo a dor que chega à consciência.
- Fatores emocionais e pelo estado de humor afetam a sensibilidade à dor. Por exemplo, uma mesma lesão pode parecer muito mais dolorosa à noite, quando nosso estado de humor aumenta as percepções da fadiga, do cansaço e dos perigos, porque somos seres diurnos, selecionados para viver durante o dia e repousar à noite.
- Experiência, história de vida e cultura afetam a percepção da dor. A memória, o conhecimento e o aprendizado da dor participam da regulação de como percebemos a dor e o medo que ela nos causa.
A dor crônica pode modificar estas estruturas por meio da plasticidade cerebral.
Por isso, a psicoterapia, o acompanhamento psicológico, técnicas de meditação e controle cognitivo podem auxiliar o controle da dor neuropática nas neurofibromatoses.
Também sabemos que a depressão e a ansiedade podem aumentar a sensação de dor. Por isso, antidepressivos e ansiolíticos podem ajudar a controlar a dor, inclusive nas neurofibromatoses.
- As características genéticas afetam a percepção da dor. Boa parte (40%) da sensibilidade à dor pode ser atribuída a fatores genéticos. Neste sentido, parece que a ausência da neurofibromina nas pessoas com NF1 aumenta a sensibilidade dolorosa de um modo geral.
- Outras causas – é possível haver outros mecanismos de dor nas neurofibromatoses que desconhecemos por enquanto. Por exemplo, na NF1 não sabemos exatamente por que os neurofibromas cutâneos raramente são dolorosos, enquanto plexiformes e nodulares muitas vezes o são. Além disso, os schwannomas raramente são dolorosos na NF2, mas são muito dolorosos na Schwannomatose. E todos estes tumores se originam da mesma célula de Schwann, na bainha dos nervos periféricos!
Em resumo, dores de diferentes intensidades e causas podem estar agindo ao mesmo tempo numa pessoa com neurofibromatose e por isso o tratamento da dor crônica e da dor neuropática geralmente é complexo e multidisciplinar.
Tratamentos para dor crônica (ESPECIALMENTE NEUROPÁTICA)
Está claro que o primeiro tratamento sempre será tentar remover a causa da dor.
Enquanto a causa está sendo removida (ou quando não é possível sua remoção) devemos usar outros procedimentos.
Costumávamos recomendar nesta página a chamada escada analgésica, baseada em orientação da Organização Mundial da Saúde, que foi reavaliada em 2010.
A partir de agora, utilizaremos uma adaptação dos procedimentos indicados pela extensa revisão realizada por Bates e colaboradores, 2019.
O primeiro passo para o tratamento adequado é diagnosticar e quantificar a dor e medir seu impacto na qualidade de vida, por meio de questionários estruturados e escalas para medir a dor e a realização de exame físico clínico por profissional experiente. Exames complementares podem ser necessários.
Depois de diagnosticada e quantificada a dor, podem ser utilizados os passos apresentados adiante.
É muito importante saber que o tratamento da dor neuropática é quase sempre MULTIDISCIPLINAR, envolvendo profissionais da saúde que orientem para a reabilitação física, apoio psicológico, higiene do sono, exercícios físicos regulares e outras ações complementares.
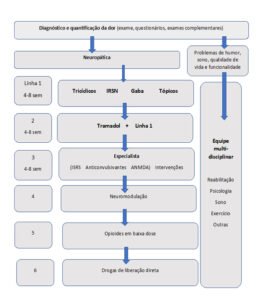
Legenda:
Antidepressivos tricíclicos (exemplos: Amitriptilina e Nortriptilina)
IRSN: inibidores da recaptação da serotonina e noradrenalina (exemplos: Duloxetina e Venlafaxina)
GABA: gabapentinoides (exemplos Pregabalina e Gabapentina)
Tópicos (exemplos: Lidocaína e Capsaicina)
Reservados aos especialistas no tratamento da dor
ISRS: inibidores seletivos da recaptação da serotonina (por exemplo, Citalopram, Escitalopram. Fluoxetina, Fluvoxamina, Paroxetina, Sertralina)
Anticonvulsivantes (por exemplo: Lamotrigina, Carbamazepina, Topiramato, Valproato)
ARNMDA: antagonistas dos receptores NMDA (por exemplo, Cetamina (ou ketamina), Tramadol e Metadona )
Intervenções, incluindo neuromodulação, opioides e drogas de liberação direta.
Observações
Antinflamatórios – Não há evidência científica de uso de antinflamatórios (não esteroides) na dor neuropática.
Canabidiol – O uso de medicamentos derivados da cannabis tem sido recomendado algumas vezes em nosso CRNF para a dor crônica, mas alguns estudos recentes (ver aqui e aqui) indicam que precisamos de mais pesquisas científicas bem controladas para afirmarmos que estes medicamentos são eficientes.
Tratamentos adjuvantes
Outros tratamentos são oferecidos, inclusive em clínicas de dor, e podem ajudar no controle da dor neuropática e da dor fantasma.
Veja abaixo alguns tratamentos propostos e sua eficiência no tratamento da dor crônica (clique nos textos em azul para abrir as referências científicas).
Atividades físicas – quando realizadas de modo regular e em intensidade adequada possuem efeito benéfico moderado, embora ainda seja baixa a qualidade das evidências científicas.
Meditação – baixa evidência sobre a dor diretamente, mas podem melhorar a depressão e a qualidade de vida.
Estimulação elétrica transcutânea (TENS) – possui evidência moderada para efeitos locais.
Terapia com espelho e realidade virtual – sem evidências científicas.
Biofeedback – efetivo para determinadas condições dolorosas.
Eletroconvulsoterapia – baixa qualidade das evidências científicas.
Acupuntura – parece ter um efeito placebo, ou seja, a pessoa ficaria sugestionada a sentir menos dor.
Massagem – apesar de muita expectativa sobre seus efeitos, ainda não temos evidências científicas de que as massagens afetem a dor neuropática.
Estimulação cerebral profunda – poucos estudos
Estimulação da medula espinhal – estudos insuficientes
Tratamentos cirúrgicos específicos para a dor crônica
Há dor crônica que pode ser curada com a cirurgia, por exemplo, por exemplo, o tumor glomus. Há maior frequência de tumor glomus em pessoas com Neurofibromatose do tipo 1 , que é um tumor geralmente benigno que surge nos corpos glomus, e pode ser removido na maioria das vezes por cirurgia (ou ser usada a ketamina quando a cirurgia é impossível).
Nas demais formas de dor crônica, sempre que a cirurgia puder remover a causa da dor, ela será prioritária. Outras vezes, técnicas cirúrgicas podem, ser usadas quando medicamentos e terapias adjuvantes falharam.
Mais informações sobre os tratamentos para a dor crônica podem ser obtidas com profissionais da saúde especialistas no tratamento da dor crônica.
Belo Horizonte, 4 de abril de 2023



 LOR 2023
LOR 2023