Convido você a ver a live realizada pela Milena com a Maria Helena, um momento de reflexão calma e animadora sobre como enfrentar as dificuldades da NF1.
Clique abaixo.
Dr Lor
Convido você a ver a live realizada pela Milena com a Maria Helena, um momento de reflexão calma e animadora sobre como enfrentar as dificuldades da NF1.
Clique abaixo.
Dr Lor

Sabemos que as pessoas com NF1 podem passar mal no calor (ver aqui), por isso fiquei feliz em saber que o Sistema Único de Saúde está se preparando para enfrentar as mudanças no clima, inclusive as ondas de calor.
Antes de trabalhar com as neurofibromatoses, fui pesquisador durante vários anos na Universidade Federal de Minas Gerais, onde trabalhei com a adaptação humana ao calor, então pretendo contribuir com o esforço do Sistema Único de Saúde (SUS), no presente Governo Lula, para o enfrentamento dos impactos das ondas de calor sobre a saúde pública brasileira.
Por isso, preparei uma cartilha para profissionais da saúde e para familiares de pessoas com NF1.
Se desejar conhecer o que são as ondas de calor e como elas afetam a sua saúde, basta clicar aqui para ver o texto completo.
Selecionei do texto completo três informações sobre as ondas de calor que podem interessar a você.
1 – O que acontece quando o corpo aumenta muito a temperatura (chamamos de hipertermia) numa onda de calor?
Não confundir com FEBRE, veja aqui.
A figura abaixo mostra sinais e sintomas que podem ser moderados (menos de 40 graus centígrados de temperatura interna) ou graves (mais de 40 graus de temperatura interna).
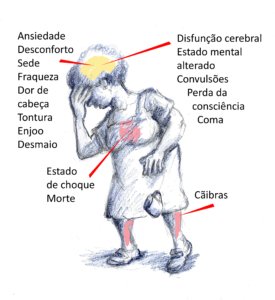
2 – Teste o seu risco
O quadro abaixo mostra um teste simples para conhecer seu risco de passar mal durante uma onda de calor.
| Condição | Sim |
| Mais de 60 anos ou menos de 10 anos | |
| Gênero feminino (dobrar pontuação se for gestante ou na menopausa) | |
| Obesidade (IMC maior que 30) | |
| Reside em região fria ou temperada | |
| Sedentarismo | |
| Mora em casa sem aparelho de ar-condicionado | |
| Possui doença cardiovascular, neurológica, renal, diabetes, câncer ou NF1 | |
| Usa algum medicamento para coração, para os rins ou neurológico | |
| Trabalha em ambiente quente e úmido ou sob o sol | |
| Já passou mal no calor (desmaio, náusea, confusão mental, “febre”, desidratação, pressão baixa) | |
| Total |
Em termos práticos, quanto maior a pontuação, maior o risco de uma pessoa apresentar hipertermia durante uma onda de calor, portanto, ela deve receber mais cuidados.
3 – E como tratar uma pessoa em estado de hipertermia durante uma onda de calor?
Os procedimentos básicos imediatos para tratamento de uma pessoa com suspeita de hipertermia moderada (temperatura interna menor que 40 graus centígrados) recomendadas pela medicina especializada em ambientes naturais, são:
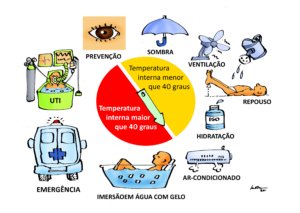
Remoção da pessoa do ambiente quente
Resfriamento natural e rápido com imersão na água fria ou molhando as roupas e promovendo ventilação
Medir a temperatura interna porque ela define se deve ou não ir para o hospital (ver abaixo comentário)
Hidratação oral
Repouso
Provavelmente estas medidas são suficientes para tratamento da hipertermia moderada, mas se houver mais recursos disponíveis, além das medidas acima, recomenda-se:
Remover a pessoa para ambiente com ar-condicionado (menor que 20 graus centígrados)
Resfriar o corpo o mais rápido que puder:
Imersão em água o mais fria possível (quanto mais rápido o resfriamento corporal, menor mortalidade e sequelas)
Se não puder ser feita a imersão, cobrir todo o corpo com compressas de gelo. Se não houver como fazer imersão ou colocar compressas de gelo, usar ventiladores sobre as roupas molhadas (menos eficiente)
Hidratar com líquidos isotônicos ou hipertônicos (para manter o volume sanguíneo e controlar as cãibras) e, se necessário, por via venosa (não há evidência de benefício em se usar infusão gelada)
Elevar as pernas e, se possível, colocar meias de compressão nas pernas para aumentar o retorno do sangue para o coração
Não usar aspirina, nem anti-inflamatórios ou outros antitérmicos!
Nota importante: como medir a temperatura interna?
A medida mais prática da temperatura interna é a medida da temperatura retal. Alternativamente, pode-se usar a temperatura timpânica ou esofagiana. Em último caso, a temperatura axilar pode ser usada, mas sabendo-se que ela pode não refletir exatamente a temperatura interna.
A medida da temperatura interna é um desafio que as equipes de saúde precisam enfrentar daqui em diante, pois há alguns anos, num estudo que fizemos em dois grandes Hospitais de Pronto Socorro em Belo Horizonte, nem mesmo a temperatura axilar era medida rotineiramente no atendimento inicial. O SUS precisa incluir esta norma em suas orientações para enfrentar as ondas de calor.
Na suspeita de hipertermia grave (temperatura interna maior que 40 graus centígrados e/ou outros sintomas graves), usar todos os recursos anteriores enquanto se transfere a pessoa para um hospital de emergências e além das medidas acima, acrescentar:
Suporte ventilatório (com oxigênio)
Suporte cardíaco (com monitorização eletrocardiográfica para detectar arritmias e da pressão arterial)
Medida da temperatura retal (ou timpânica) (maior que 40 graus confirma a gravidade)
Monitorar o volume e a cor da urina para avaliar o estado de hidratação
No hospital deve receber cuidados intensivos porque podem desenvolver as seguintes complicações:
Estado de choque com falência múltipla de órgãos
Encefalopatia (tremores, confusão mental e agressividade durante resfriamento rápido)
Insuficiência respiratória
Lesão hepática e renal agudas
Rabdomiólise (lesão muscular grave)
Coagulação intravascular disseminada
Isquemia intestinal com septicemia
Os detalhes do tratamento intensivo fogem ao objetivo deste texto, mas todas as medidas terapêuticas devem ser tomadas enquanto se continua o resfriamento do paciente. Até a temperatura interna (retal) atingir 38,3 a 38,8 graus centígrados, o resfriamento ativo deve ser mantido (ver detalhes aqui).
As equipes de emergência precisam criar condições técnicas (salas especiais e ambientes adaptados) que permitam o resfriamento por imersão em água gelada enquanto outros procedimentos são realizados.
A equipe médica deve também fazer o diagnóstico diferencial com: hipoglicemia, epilepsia, doença do sistema nervoso central, hiponatremia, hipernatremia, edema cerebral de alta altitude, infecção grave, alteração endócrina grave e ingestão de drogas.
Veja mais informações no texto completo AQUI.
Portanto, cuidemos da vida.
Dr Lor

Tenho a satisfação de receber no nosso blog uma pessoa que está sendo conhecida na comunidade NF pelo seu excelente trabalho de divulgação científica e humanitária sobre as NF no canal Enfermeira Rara, do qual tive a oportunidade de participar ontem (ver abaixo).
Com a palavra, Milena!
Dr Lor
Olá! Sou a Milena, enfermeira, tenho Neurofibromatose tipo 1, motivo da minha pesquisa de mestrado, sou mestre em Psicologia da Saúde, além de autora do livro “Neurofibromatose: Mapeamento de Associações, Instituições e Serviços Existentes no Brasil”.
Sou natural de Votuporanga, interior de São Paulo, e atuo há mais de 10 anos na área da Saúde Mental, trabalhando em um CAPS II. Posso dizer que, além da minha paixão pela psiquiatria, também me descobri encantada pelo universo da genética.
Durante minha participação em grupos de WhatsApp, percebi a grande necessidade de levar informações baseadas em ciência, com o apoio de profissionais renomados no assunto, para um público mais amplo.
Foi então que enxerguei a oportunidade de usar a internet como ferramenta de divulgação* e de apoio às pessoas que convivem com a Neurofibromatose, uma doença rara e ainda pouco conhecida — inclusive entre profissionais da saúde.
Em uma conversa com um amigo de trabalho, surgiu a ideia de criar um canal no YouTube, e assim nasceu o meu “xodó”: o canal *Enfermeira Rara*, um espaço criado com muito carinho para compartilhar conhecimento, histórias reais e experiências transformadoras.
No meu canal você vai encontrar lives com especialistas, depoimentos pessoais e conteúdos educativos sobre o universo das doenças raras.
Meu objetivo é informar, acolher e conectar pessoas — pacientes, familiares e profissionais — que desejam aprender mais sobre essa causa.
Lá, conversamos sobre Neurofibromatose de forma leve, acessível e embasada, compartilhando informações, histórias de vida, depoimentos e lives com profissionais de excelência que dominam o tema.
Tem sido uma experiência incrível! O canal me proporcionou conhecer pessoas maravilhosas, dispostas a fortalecer essa rede, e profissionais comprometidos* em divulgar conhecimento de qualidade.
Se você ainda não conhece, *corre lá e se inscreva*! LINK
Você vai encontrar vídeos com meus depoimentos pessoal, além de todas as lives gravadas, repletas de conteúdo e aprendizado.
Aproveito para agradecer a todos os profissionais que aceitaram o meu convite até aqui, ao apoio da minha família e, especialmente, ao John, que está por trás das câmeras tornando tudo isso possível.
Com carinho,
Rosângela Milena da Silva
Enfermeira Rara
Veja a live de ontem
Uma parte das pessoas com NF1 apresenta ossos mais fracos do que a população sem NF1 de mesmo sexo e idade. A Vitamina D participa da formação sadia dos ossos, então, há muitos anos temos nos preocupado se os níveis de Vitamina D nas pessoas com NF1 estão adequados.
Com esta mesma preocupação, um grupo de pesquisadoras italianas, lideradas pela Dra. Claudia Riccardi, publicaram o maior estudo já realizado sobre este assunto (454 referências bibliográficas) na revista Cancer, com o título: “Compreendendo as atividades biológicas da Vitamina D na Neurofibromatose do tipo 1: novos entendimentos sobre o desenvolvimento da doença e métodos de tratamento” (clique aqui para ver aqui ao artigo completo em inglês).
O artigo reúne praticamente tudo que sabemos sobre Vitamina D e NF1, inclusive cita três estudos realizados em nosso Centro de Referência em Neurofibromatoses, abordando as relações da Vitamina D com neurofibromas, com a redução da força muscular e com os ossos mais fracos.
A principal conclusão deste vasto estudo é que ainda precisamos estudar melhor o papel da Vitamina D na NF1, mas há conhecimentos suficientes para justificar a atenção clínica permanente com o objetivo de manter níveis adequados de Vitamina D no sangue das pessoas com NF1. Para isso, devemos utilizar dietas adequadas, banhos de sol e, se não forem suficientes, suplementação medicamentosa supervisionada por profissionais da saúde.
Ver em nossas páginas mais informações sobre a dieta, banhos de sol e suplementação de Vitamina D.
Dr Lor
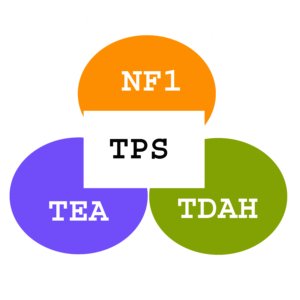
Um estudo científico bem conduzido na Austrália pelo grupo da Dra. Kathryn N. North avaliou o comportamento de crianças e adolescentes com neurofibromatose do tipo 1 (NF1), transtorno no espectro do autismo (TEA) e transtorno de déficit de atenção e hiperatividade (TDAH). (Ver aqui artigo completo em inglês) .
As equipes do CRNF e da AMANF estão preparando um texto explicativo sobre os resultados do estudo e sua aplicação prática em nossa vida. Em breve ele estará disponível em nossa página, mas quero adiantar que o estudo observou que as crianças e adolescentes com NF1, TEA e TDAH apresentam em comum comportamentos causados pelo transtorno do processamento sensorial (TPS).
O Transtorno de Processamento Sensorial são as dificuldades de uma criança para processar os diferentes estímulos que vêm do ambiente e da sociedade de forma a se comportar adequadamente naquela situação.
O que é o processamento sensorial?
O processamento sensorial é a capacidade do sistema nervoso de detectar, integrar, modular e interpretar todas as informações captadas pelos diversos sensores que foram ativados pelos estímulos que nos chegam do ambiente e do nosso próprio corpo. As informações sensoriais processadas no sistema nervoso central, que permitem nossa adaptação ao ambiente, são:
A integração de todas estas informações sensoriais é que nos permite reagir adequadamente às variações internas e do ambiente. Elas são utilizadas pelo sistema nervoso para que possamos perceber de forma contínua o nosso próprio corpo num determinado ambiente físico, assim como os indicadores e regras sociais para que nosso comportamento seja adequado a cada momento em cada grupo de pessoas ou sociedade.
Em breve daremos mais informações sobre este transtorno e como podemos melhorar as pessoas com NF1 e TPS.
Dr Lor

Vi o filme “Um homem diferente”, que foi celebrado nos festivais de cinema de 2024 como uma comédia atípica, intrigante e impactante, sobre Edward, um personagem que nasceu com grande deformidade na face e que se submete a uma experiência de ficção científica para corrigir seu problema e se tornar um indivíduo semelhante aos demais.
O personagem fictício Edward – tímido, solitário e inseguro – é representado pelo ator Sebastian Stan, que usa uma maquiagem complexa para simular os tumores na face para se tornar parecido com outro personagem do filme, Oswald, representado por Adam Pearson, um ator inglês que na vida real é portador da doença genética Neurofibromatose do tipo 1 (NF1).
Oswald, ao contrário de Edward, é uma pessoa descontraída, bem-sucedida, sedutora, fascinante, com amigas, amigos e muitos amores, apesar da deformidade facial.
Apesar do ator Adam Pearson possuir, de fato, NF1 (junto com seu irmão gêmeo Neil), o filma não menciona a doença em nenhum momento e a história mistura fantasia e realidade sobre o que significa uma grave deformidade facial numa sociedade dominada pelo mito da beleza (ver aqui).
A fantasia do filme, pelo menos até esse momento, consiste na possibilidade de restauração completa da face de Edward, transformando-o no bonitão Sebastian Stan. Neste sentido, o filme parece mais ficção científica e é preciso ver as cenas da segunda metade do filme para a gente desconfiar porque foi considerado uma comédia.
A trama de sedução e ciúme entre os personagens e a vizinha diretora de teatro é narrada de forma caricatural e deve ter chamado a atenção pública porque as deformidades faciais – fictícia na maquiagem de Edward e a real na pele de Adam Pearson – despertam em todos nós espectadores sentimentos antagônicos: de um lado, a reação instintiva de medo e espanto – diante de um rosto extremamente diferente, – do outro, a empatia civilizatória que vai sendo despertada pela consciência de que por trás daquela “máscara” existe um ser humano.
No cerne, sem dar spoiler, o filme coloca em discussão se é possível alguém com uma deformidade corporal grave levar uma vida como as demais pessoas, sem rejeição, sem isolamento e sem bullying ou hostilidade.
Estive pessoalmente com Adam Pearson num congresso sobre neurofibromatose na Flórida, enquanto ele conversava com nosso querido Dr. Vincent Riccardi, o qual elogiava a camiseta que Adam usava com os dizeres “ASK ME”, estimulando as pessoas a perguntarem a ele o que havia com sua face, abrindo assim uma oportunidade de conversarem a respeito da doença e quem sabe, nesse diálogo, ser diminuído o preconceito das pessoas.
Esta camiseta do ator inglês é um indício de que a “vida absolutamente normal” do personagem Oswald no filme “Um homem diferente” não deve ser tão comum ou fácil para os portadores de deformidades corporais.
Na nossa experiência com mais de 3 mil famílias atendidas em nosso Centro de Referência em Neurofibromatoses do Hospital das Clínicas da Universidade Federal de Minas Gerais, temos visto que algumas pessoas com NF1 apresentam deformidades faciais com gravidade semelhante àquela de Adam Pearson, embora sejam raríssimas e geralmente unilaterais.
No entanto, para além do acometimento estético e independentemente dele, a NF1 altera profundamente o comportamento das pessoas acometidas pela doença, sendo frequentes nelas a ansiedade, a depressão, o retraimento social e a solidão (ver aqui mais informações sobre isso). Portanto, na vida real, as pessoas com NF1 são mais parecidas com o personagem Edward do que com o personagem de sucesso Oswald no filme.
Quando associamos as dificuldades psicológicas com a segregação social causada pelas deformidades, o resultado para as pessoas com NF1 é uma vida solitária e com poucas possibilidades de realização pessoal nas condições sociais atuais.
Em conclusão, pareceu-me que o recado geral do filme é uma versão longa da ideia de que a beleza está no interior, e que você pode ser uma pessoa amada por todos se você se amar de verdade, ainda que seja portador de uma deformidade facial que o afasta do mundo ao seu redor.
Talvez seja difícil comprovar esta fantasia otimista diante da realidade cruel da sociedade em que vivemos: individualista, competitiva, exclusiva e baseada no mito de beleza.
Além disso, o filme comete um grave erro do ponto de vista de aconselhamento genético e planejamento familiar, pois mostra o personagem Oswald tendo vários filhos com mais de uma mulher, sem qualquer preocupação com a hereditariedade da NF1, a qual é uma doença genética dominante e apresenta a probabilidade de transmissão da mutação para metade dos filhos ou filhas.
Portanto, é um filme que deve ser visto com reservas, pois apresenta discursos baseados no senso comum e não nos conhecimentos científicos que atualmente estão disponíveis para milhões de pessoas com NF1 ao redor do mundo.
No entanto, as pesquisas científicas precisam continuar para que um dia sejamos capazes, de fato, de corrigir plenamente os problemas estéticos, psicológicos e comportamentais das pessoas com NF1.
Dr. Luiz Oswaldo Carneiro Rodrigues

Muitas famílias me perguntam como podem ajudar suas crianças com NF1 a superarem suas dificuldades cognitivas.
Diversas equipes de cientistas estão procurando esta resposta e temos feito grandes progressos na compreensão dos principais problemas neurológicos causados pela NF1.
Por exemplo, neste ano de 2025, Gamze Kaplan e colaboradores publicaram seu estudo sobre a interação entre os pais e a criança com NF1 e TDAH (Transtorno de Déficit de Atenção e Hiperatividade) numa revista científica (ver aqui artigo completo em inglês).
Os resultados mostraram que a NF1 e o TDAH são problemas diferentes, mas que apresentam semelhanças no curso do desenvolvimento. Os processos neuro divergentes em ambas as condições começam no primeiro ano, alterando tanto o comportamento do bebê quanto a maneira como os pais respondem a ele, porque os pais vão reduzindo as oportunidades sociocomunicativas para o desenvolvimento social do cérebro.
Este estudo comparou as interações pais-bebês em três grupos de crianças de 10 a 14 meses de idade:
A hipótese dos autores era de que os bebês com NF1 (Grupo 1) e bebês com TDAH (Grupo 2) mostrariam menos atenção dirigida aos seus pais e menos interação mútua entre pais e bebês, comparados aos bebês com desenvolvimento típico (Grupo 3). A suspeita era de que a atenção aos pais seria mais baixa em bebês com NF1 e que a vivacidade e o afeto negativo seriam maiores em bebês com NF1 e TDAH.
Os pais e seus bebês com NF1, TDAH e DT foram filmados durante as interações de brincadeiras livres e codificados usando escalas de classificação validadas.
Os resultados mostraram, que a interação pais-bebês dos bebês com NF1 e TDAH foram diferentes entre si e diferentes das crianças com desenvolvimento típico (DT).
O grupo NF1 mostrou relativamente menos interações mútuas (pais-bebês) do que o grupo TDAH, e respostas muito mais baixas às ações dos pais do que o grupo DT, enquanto os bebês TDAH eram mais animados e mostraram menos afetos negativos em relação aos outros grupos.
A maioria dos efeitos principais persistiu ao longo do tempo.
Embora seja necessário um acompanhamento de longo prazo em amostras maiores, estes resultados mostram como crianças com condições de neurodesenvolvimento alteradas apresentam experiências sociais distintas no primeiro ano de vida, o que pode impactar todo seu desenvolvimento cognitivo, psíquico e social ao longo da vida.
Na minha opinião, estes resultados reforçam a necessidade de que pais e cuidadores de crianças com NF1 fiquem atentos para esta baixa interação social provocada pela doença e tentem estimular estas crianças de forma planejada e consistente ao longo do seu desenvolvimento.
E a neuromodulação?
Com esta intenção em mente, algumas famílias têm perguntado se as técnicas de “neuromodulação” poderiam ser eficientes para estimular o desenvolvimento de suas crianças com NF1.
Sob o nome “neuromodulação” existem técnicas diferentes (ver anexo abaixo). Todas elas enfrentam dificuldades para padronização dos protocolos, para a quantificação de dose-resposta, e para a identificação de biomarcadores eficazes, assim como o estímulo em áreas extensas pode dificultar a localização exata dos efeitos.
E na NF1?
Até o presente, existe um grupo de pesquisadores testando a eletroestimulação transcutânea em crianças com NF1 e este grupo vem publicando seus resultados.
Em 2022, publicaram um artigo “Non-invasive brain stimulation modulates GABAergic activity in neurofibromatosis 1 — Scientific Reports (2022), com 31 adolescentes com NF1 (11–18 anos), no qual não houve melhora comportamental sustentada ao final da estimulação (desempenho durante a estimulação chegou a piorar).
Em 2025, publicaram “Non-invasive brain stimulation reorganises effective connectivity during a working memory task in individuals with NF1 — NeuroImage: Reports (2025), que não mostrou ganho cognitivo clinicamente relevante.
Finalmente, no congresso do CTF deste ano ( 2025), apresentaram um resumo que a Dra. Pollyanna Barros Batista comentou neste blog: ver aqui.
Na minha opinião, estas técnicas ainda são experimentais nas pessoas com NF1 e não há evidência de que já possam ser utilizadas como terapias efetivas.
Em conclusão, o melhor tratamento que dispomos ainda é a atenção cuidadosa de mães, pais e cuidadores para as necessidades diárias de cada criança com NF1.
Uma atenção que supere o retorno afetivo menor que as crianças com NF1 podem devolver a seus pais.
Uma atenção permanente e amorosa que procure ajudar cada uma delas a atingir seu potencial de felicidade, bem-estar e realização pessoal em sua vida.
Dr LOR
Anexo
Técnicas de neuromodulação

Opinião pessoal
Tenho observado que muitas crianças e adolescentes com NF1 usam celulares e redes sociais por muitas horas todos os dias e de forma pouco controlada pelas mães e pelos pais.
O uso de celulares e redes sociais são muito perigosos para crianças e adolescentes (ver aqui informações científicas sobre isso): eles e elas estão adoecendo mentalmente, com mais angústia, ansiedade, agressividade, depressão, automutilação e tentativas de suicídio.
Ainda não há estudos científicos sobre celulares e redes sociais em crianças com NF1, mas já sabemos as crianças e adolescentes com NF1 apresentam mais ansiedade, baixa autoestima, isolamento social e depressão do que as crianças sem NF1.
Assim, o bom senso nos faz tomar mais cuidado ainda com os celulares nas mãos das crianças com NF1.
Série Adolescência
Para compreender melhor a profundidade do problema, recomendo que vejam a série da Netflix “Adolescência”, que mostra o impacto das redes sociais sobre o comportamento de um menino, um garoto comum, numa sociedade machista.
Entre as várias questões importantes despertadas pela série, uma delas poderia ser a falta de modelos de masculinidade não-machista para as novas gerações.
Mesmo nós, os que tentam desconstruir o machismo estrutural no qual fomos constituídos como homens, ainda não somos exemplos do novo homem.
Além disso, pode ser que ainda não haja muitos homens desprovidos dos valores machistas na atual sociedade capitalista, que funciona às custas da meritocracia e das desigualdades estruturadas em gênero, raças e fronteiras.
Mas provavelmente seria mais inspirador para meninos e adolescentes se eles tivessem mais exemplos de homens não-machistas para se espelharem do que somente serem estimulados a não se comportar como os machões atuais.
Então, como seriam estes exemplos dos novos homens?
Numa conversa, Dra. Luíza de Oliveira Rodrigues e eu ficamos imaginando que este novo homem poderia ser alguém que, por exemplo:
– Considera o trabalho de reprodução da vida o mais importante
– Escuta e não só fala
– Nunca usa da sua força para impor sua vontade
– Sabe que é mortal e reconhece o valor da própria vida e da vida das outras pessoas
– Busca amar e ser amado e não o poder ou status
– Aprende que não existe bem estar próprio sem a participação das outras pessoas
– Descobre que a competição é solidão e a cooperação é encontro
Com isso, esse “novo homem” seria uma pessoa solidária, empática e respeitosa para com todas as demais.
Mas, veja só! – estas qualidades não são exclusivas de qualquer sexo ou gênero.
São as qualidades humanas fundamentais.
Uma sociedade baseada nestes valores será igualitária em termos de gênero.
Viva!
PS: Se desejar, mais informações sobre este tema veja aqui Mania de músculos e aqui Precisamos de mais professores homens professores no ensino básico

Trago hoje mais um dos capítulos escritos para a Edição Comemorativa dos 20 anos do CRNF, a ser lançada em dezembro de 2024, com o texto do médico e nosso amigo e colaborador de longa data Dr. Nikolas Mata-Machado, professor de pediatria e com grandes contribuições para o tratamento das crianças com NF1 e problemas neurológicos. Muito obrigado, em nome de toda a equipe do CRNF.
Dr. Lor
Nikolas Mata-Machado
Médico, PhD Professor Assistente de Pediatria
Chefe da Neurologia Pediátrica – Diretor da Clínica de Neurofibromatose
Universidade de Chicago – Estados Unidos da América
As convulsões são uma complicação bem conhecida da neurofibromatose tipo 1 (NF1), com prevalência relatada entre 3,8% e 6,4% da população [1]. No entanto, esta prevalência pode ser superestimada devido a um viés de apuração.
Em pessoas com NF1, as crises convulsivas parciais complexas são as mais comuns, mas também são descritas convulsões generalizadas primárias, espasmos infantis e crises febris. A idade média de início das convulsões é na infância.
Um estudo indicou que até 64% dos pacientes com NF1 apresentavam lesões estruturais no encéfalo que originavam as convulsões [2]. Contudo, as amostras de pacientes estudadas eram relativamente pequenas e focadas em pacientes pediátricos, o que pode ter excluído convulsões em pessoas mais velhas. Para comparação, na população em geral (sem NF1), a prevalência de convulsões nos países da Europa, além dos Estados Unidos, Canadá e Japão, é de 0,68%, com uma incidência de 44 por 100.000 pessoas, apresentando picos de incidência na primeira infância e após os 65 anos [3]. As crises parciais complexas são as mais frequentes.
Em pacientes com NF1, a experiência sugere que as convulsões são bastante comuns e podem ocorrer em todas as idades. Muitas vezes, as convulsões são sutis e passam despercebidas, com eletroencefalogramas (EEG) de rotina normais. Em muitos casos, é necessário monitoramento prolongado de vídeo EEG para capturar anormalidades.
A baixa incidência relatada de convulsões pode ser atribuída à baixa disponibilidade de monitoramento prolongado de EEG. Em pacientes com NF1, 42% das convulsões começam antes dos 5 anos de idade, conforme observado por Korf et al. [4], que relatam uma idade média de início de 8,1 anos. Convulsões em pessoas com NF1 após os 4 anos também foram documentadas, o que contrasta com a queda acentuada nas convulsões após essa idade na população em geral.
A causa exata das convulsões na maioria das pessoas com NF1 é desconhecida, mas tumores e doenças vasculares associados à NF1 podem ser causas em apenas um pequeno número de casos. Pesquisas recentes sugerem que pacientes com atraso no desenvolvimento, autismo, dificuldades comportamentais e problemas emocionais graves têm um risco maior de convulsões [5]. Recomenda-se , então, gravações prolongadas de vídeo EEG para avaliar esses crianças.
Alguns dados indicam que uma pequena porcentagem de pessoas com NF1 possui outros membros da família com convulsões, sugerindo que a tendência para convulsões está relacionada à NF1 e não a uma predisposição genética separada para convulsões [6].
Referências
[1] Creange A, Zeller J, Rostaing-Rigattieri S, et al. Neurologic complications of neurofibromatosis type 1 in adulthood. Brain 122:473-481, 1999.
[2] Jennings MT, Bird TD. Genetic influences in epilepsies. Review of the literature with practical implications. Am J Dis Child 135:450-7, 1981.
[3] Hauser AW, Annegers JF, Kurland LT. Incidence of epilepsy and unprovoked seizures in Rochester Minnesota: 1935-1984. Epilepsia 34:453-468, 1993.
[4] Korf BR, Carrazana E, Holmes GL. Patterns of seizures observed in association with neurofibromatosis 1. Epilepsia 34:616-620, 1993.
[5] Creange A, Zeller J, Rostaing-Rigattieri S, et al. Neurologic complications of neurofibromatosis type 1 in adulthood. Brain 122:473-481, 1999
[6] Szudek J, Birch P, Riccardi VM, etal. Associattion of clinical features in neurofibromatosis 1 (NF1). Genet Epidemiol 19:429-39, 2000.

Apresento hoje mais um dos capítulos escritos para a Edição Comemorativa dos 20 anos do CRNF, a ser lançada em dezembro de 2024, com o texto da psicóloga Katie Moraes de Almondes, que amplia as questões apresentadas recentemente pela sua colega Alessandra Craig Cerello. Nesse artigo Katie nos mostra um caminho importante a ser investigado para melhorarmos a qualidade de vida das pessoas com NF1. Muito obrigado, em nome de toda a equipe do CRNF.
Dr. Lor
Katie Moraes de Almondes
Professora Associada do Departamento de Psicologia
Programa de Pós-graduação em Psicobiologia
Universidade Federal do Rio Grande do Norte
Coordenadora do Ambulatório do Sono e
Ambulatório de Narcolepsia e Apneia do Sono infantil
Hospital Universitário Onofre Lopes da UFRN)
A neurofibromatose tipo I (NF1) é uma doença genética autossômica dominante rara, com prevalência de 1:3.000 nascidos vivos, que acontece devido a mutações heterozigóticas do gene NF1 e, subsequente, haploinsuficiência do produto proteico codificado neurofibromina (Kresak & Walsh, 2016). O diagnóstico geralmente é feito na infância e é estabelecido pela identificação de dois ou mais dos seguintes critérios clínicos: mais de seis manchas café com leite, sardas axilares ou inguinais, dois ou mais neurofibromas cutâneos ou um neurofibroma plexiforme, dois hamartomas de íris (Nódulos de Lisch), gliomas do nervo óptico, displasias esqueléticas e história de parente primário com a doença e painel genético contendo uma variante patogênica no gene NF1 (Souza et al, 2009).
A NF1 pode afetar diversos órgãos e sistemas. O sistema nervoso central (SNC) é, frequentemente, afetado nas crianças com NF1 com impactos que envolvem alterações cognitivas, comportamentais, distúrbios da fala (Cosyns et al, 2010), problemas motores (Vogel, Gutmann & Morris, 2017), enxaqueca, doenças cerebrovasculares, tumores cerebrais, epilepsias, estenose aquedutal e lesões cerebrais de alto sinal na ressonância magnética ponderada em T2 (Santoro et al, 2018).
Outrossim, alguns estudos sugerem que a NF1 também está associada aos distúrbios de sono, mas os resultados clínicos na literatura são escassos e, ao mesmo tempo, controversos. Alguns estudos apontam que há um indicativo de alta prevalência de distúrbios de sono entre crianças e adolescentes com NF1, enquanto outros defendem que a incidência é similar para a população pediátrica em geral (Maraña et al, 2015).
Esses distúrbios, muitas vezes, são queixas de sono relatadas subjetivamente pelos próprios pais, por uma percepção que tende a superestimar ou subestimar, por serem acordados durante a noite e, frequentemente, não se recordarem com exatidão o padrão do sono, pois a percepção da queixa da criança estar influenciada pela queixa dos pais sobre o próprio despertar. Não obstante, as queixas quando relatadas não são diagnosticadas a partir de critérios clínicos, o que leva a mais imprecisão sobre o padrão de sono das crianças e adolescentes com NF1. Isso é corroborado, principalmente, pelos poucos artigos que trazem a conclusão de disturbios de sono baseados em questionários gerais pediátricos (Johnson, Wiggs, Stores, & Huson, 2005; Maraña et al, 2015). Somado a isso, a anamnese pediátrica, na maioria das vezes, não inclui avaliações sobre padrões e hábitos de sono.
É ponto pacífico na literatura que o sono insuficiente e inadequado em crianças está ligado a uma série de resultados adversos para a saúde, como fadiga diurna (Lehmkuhl et al, 2008), atraso no desenvolvimento neuropsicomotor (Smaldone, Honig, & Byrne, 2007), desempenho cognitivo reduzido (Gruber et al, 2014), sistema imunológico comprometido (Smaldone, Honig, & Byrne, 2007) e obesidade (Fatima, Doi, & Mamun, 2015).
Além disso, problemas persistentes de sono na infância podem reduzir o bem-estar da família e aumentar o risco de desenvolvimento de dificuldades cognitivas e comportamentais na adolescência e na idade adulta, como transtornos de ansiedade, depressão, comportamento agressivo e dificuldades de atenção (Gregory et al, 2008). O diagnóstico e o tratamento dos problemas do sono são essenciais para garantir um desenvolvimento saudável.
Tomando como base as limitações supracitadas e os impactos derivados de uma associação entre NF1 e distúrbios de sono, em 2005, Johnson et al. (2005) (17) investigaram, através de questionários com 64 crianças com NF1, de 3 a 18 anos, os padrões e comportamentos de sono, e concluíram que havia maior prevalência de parassonias NREM relatadas (terrores noturnos e sonambulismo). Licis et al. (2013), (20) também, investigando o sono de 129 crianças com NF1 e 89 irmãos não afetados, com idades entre 2 e 17 anos, através de um questionário, relataram distúrbios no início e manutenção do sono com presença de despertares noturnos.
Diante dos dados escassos e derivados de outros países, em 2023, no Brasil, conduzimos o primeiro estudo que avaliou padrões, hábitos e problemas de sono em crianças com NF1. Através de um estudo transversal com 41 crianças, sendo 28 (68%) crianças na faixa etária de 06 a 12 anos e 13 (32%) na faixa etária de 01 a 05 anos, recrutadas, voluntariamente, através da Associação Mineira de Apoio às Pessoas com Neurofibromatose e grupos de apoio do Centro de Referência em Neurofibromatose, Brasil (Almondes et al, 2023).
Nossos resultados apontaram que as crianças com NF1 apresentavam horários tardios de ir para a cama, despertares noturnos frequentes, dormiam menos de dez horas por noite, e manifestavam resistência em ir para a cama, características de um quadro de insônia comportamental (ICSD-3-TR).
Importante assinalar que os horários tardios de ir para a cama apresentam correlação com maior tempo para adormecer e menor tempo total de sono (Mindell, Meltzer, Carskadon e Chervin, 2009). Acerca da resistência em ir para a cama, Sadeh, Tikotzky e Scher (2010) sugerem que a presença parental no momento de dormir da criança pode favorecer os despertares e dificultar a independência para adormecer. Ademais, a criança pode associar o início do sono com a presença dos pais e só conseguir adormecer na presença destes, tendo dificuldade em dormir sozinha.
Acreditamos que os problemas de sono em crianças com NF1 podem decorrer do comportamento dos pais, como ficar próximos à cama da criança devido aos cuidados rotineiros que desempenham em função da doença, e aumentar a superproteção devido à NF1, desfavorecendo a independência da criança no momento de dormir. Assim, esse comportamento pode reforçar a manutenção e perpetuação da queixa de adormecer apenas na presença de um adulto (Almondes et al, 2023).
Nossa amostra revelou um uso elevado de dispositivos eletrônicos à noite, principalmente televisão e celular. O uso desses dispositivos causa agitação psicológica e fisiológica, associada à resistência para dormir, atraso no horário de dormir e ansiedade. Além disso, a exposição a luzes brilhantes, especialmente a luz azul das telas, pode suprimir a produção de melatonina (Aishworiya et al., 2018; Hale & Guan, 2015).
Esses fatores, somados à probabilidade de as crianças seguirem os horários dos adultos, não terem uma rotina de sono definida e não serem independentes para adormecer, podem contribuir para resistência em ir para a cama, horário de sono tardio e menor duração do sono. Mindell et al. (2009) já apontaram que crianças sem uma rotina de sono consistente ou que seguem a rotina dos adultos tendem a dormir menos.
A partir de 2016, exames polissonográficos têm sido fortemente recomendados e considerados obrigatórios para neurofibromas plexiformes das vias aéreas em indivíduos com NF1 (Plotkin et al, 2016) (19), apesar de não ser uma prática rotineira em nosso país. Dados de Carotenuto et al (2023), seguindo essa diretriz, evidenciaram que a macroestrutura do sono de crianças com NF1 sem comorbidades neurocognitivas apresentaram redução nos parâmetros de duração do sono, da eficiência do sono e do estágio N2. Além disso, o número de despertares por hora, despertar após o início do sono (WASO) e eventos respiratórios como Índice de Apneia e Hipoapneia resultaram maiores nas crianças com NF1 em comparação com crianças saudáveis. Esses dados reforçam os dados encontrados através de medidas subjetivas.
Considerações Finais:
Ainda temos um longo caminho a percorrer quando se fala de alterações de sono na NF1.
Muitas pesquisas precisam avançar e alavancar avaliações mais acuradas e preconizadas como protocolo recomendável. Na sequência, é importante assegurar manejo terapêutico adequado e eficiente para os distúrbios de sono na população com NF1.
Alcançar quantidades adequadas de sono é importante para o desenvolvimento social, emocional, comportamental e acadêmico das crianças e adolescentes.
Na idade pré-escolar, a duração do sono tem um efeito ainda mais importante, uma vez que está intrinsecamente associada a fatores como crescimento, desenvolvimento cognitivo e comportamental, maturação do sistema nervoso central e manutenção do balanço energético.
Políticas públicas para o público com NF1 precisam ser melhor delineadas, e a pauta de sono merece atenção especial.
Os profissionais de saúde devem ser melhor capacitados nessa área e interface para promover saúde biopsicossocial para esse público.
Referências